血液腫瘤科/細胞治療中心/台灣細胞免疫醫學會 陳駿逸醫師
胎兒甲種蛋白(AFP)是廣泛認可的肝細胞癌及卵黃囊腫瘤的腫瘤標記物。製造或會產生胎兒甲種蛋白的胃癌是一種罕見但高度惡性的胃癌亞型,與預後不佳有關係。會製造胎兒甲種蛋白(AFP)的胃癌其特徵是血清或免疫組織化學染色中可以檢測到 AFP 陽性,可能伴隨肝細胞的分化。
近年來,分子生物學與治療藥物的進展,使人們對會製造胎兒甲種蛋白(AFP)的胃癌的理解更為深入。然而,其腫瘤形成及侵襲性轉移的機制仍不明朗。
AFP是一種胚胎血清糖蛋白,首次於 1956 年被鑑定。AFP主要是由卵黃囊上皮和胎肝產生,較少量則由胚胎胃腸上皮合成[。臨床上,AFP 升高被廣泛用於預測肝細胞癌及胚胎腫瘤。在某些病理狀況下,例如肝炎、肝硬化、原發性肝細胞癌、卵黃囊腫瘤、畸胎瘤及生殖系統惡性腫瘤,AFP 水平可以顯著升高。然而,AFP 升高也可能在不同程度上發生於源自於內胚層器官的惡性腫瘤,包括胃腸道癌、胰臟癌、膽囊癌及肺癌。
會分泌 AFP 的消化道腺癌,可以起源於胃腸道的任何部位,且具有相似的臨床病理特徵。會分泌 AFP 的消化道腺癌的系統性分析顯示,原發腫瘤可能發生於食道(占比0.6%)、胃(83.1%)、十二指腸(1.1%)、迴腸(0.6%)、闌尾(0.6%)、大腸(5.1%)及直腸(7.9%),其中肝狀分化為主要病理特徵。此外,我們分析了 AFP 對會分泌 AFP 的消化道腺癌之預後的影響,發現 AFP 表現過高在食道、胃、結腸及直腸癌中作為較差的預後指標。總結來說,會分泌 AFP 的消化道腺癌的預後比一般腸胃道之腺癌更差,
會製造胎兒甲種蛋白(AFP)的胃癌被定義為是胃癌的一種亞型,其特徵是血清或腫瘤組織中 AFP 水平出現異常升高,可能伴隨肝細胞的分化,但排除其他可能導致 AFP 升高的疾病,例如:肝炎、肝硬化、肝細胞癌及生殖細胞腫瘤,
對會製造胎兒甲種蛋白(AFP)的胃癌患者之腫瘤樣本的免疫組織化學染色,證明 AFP 在細胞質中表達並分泌於基質中,暗示其在調節胃癌腫瘤微環境中扮演的角色。會製造胎兒甲種蛋白(AFP)的胃癌約佔胃癌病例的 1.3%至 15%,特徵為高度侵襲性。 肝臟轉移的傾向,預後不佳。近期有研究者提出一套結合組織學特徵與 AFP 產生特徵(基於血清與免疫組織化學)的新型分類系統。此方法可以提升診斷準確度,並支持更明智的治療決策。
AFP 在癌症發病機制中扮演著多重角色,促進腫瘤生長、抗細胞細胞失位、轉移及免疫迴避,使其成為會製造胎兒甲種蛋白(AFP)的胃癌中重要的生物標記及潛在治療目標。AFP 的惡性行為主要由其 AFP 受體所介導,AFP 受體在各種腫瘤細胞上表達,調節腫瘤訊號轉導。AFP 透過結合肝癌細胞上的 AFP 受體促進腫瘤的增殖,活化 cAMP-PKA 訊號通路並誘導鈣離子流入。此活化促進癌基因如 c-fos、c-jun 及 n-ras 的表現,促進腫瘤的生長。此外,AFP 透過干擾關鍵凋亡途徑,包括 Caspase-3、Fas/FADD 及 RAR 途徑,抑制細胞凋亡,從而延長腫瘤細胞存活的時間。
AFP會進一步促進腫瘤侵襲與轉移,透過上調 CXCR4、MMP-2/9、角蛋白 19 及 EpCAM,這些皆與癌細胞遷移及侵襲有關。同時,它也會上調 VEGF 和 VEGFR,促進血管新生,為腫瘤提供生長所需的血液供應,並進一步將癌細胞擴散至遠處。AFP 與 PTEN 共定位,透過 AKT(Ser473)磷酸化途徑誘導 CXCR4 表達,從而促進細胞遷移與入侵。此外,AFP 透過活化 PI3K-AKT-mTOR 途徑並抑制自噬,使腫瘤細胞對治療反應減弱,有助於產生化療抗藥性。 AFP 同時透過抑制樹突狀細胞的成熟、減少抗原呈現及抗腫瘤細胞激素分泌(如 IL-12 與 TNF-α)來損害免疫反應,影響 T 細胞分化並下調 NK 細胞上的 NKG2D 表現。
在其他方面,腫瘤細胞的 AFP 可能削弱抗腫瘤 CD8+T 細胞,並透過誘導耐受性樹突狀細胞,誘導 NK 細胞死亡。此外,AFP 促進調控 T 細胞(Tregs)的擴增,抑制免疫監控],並促進巨噬細胞向 M2 樣表型極化,抑制腫瘤細胞的吞噬作用。
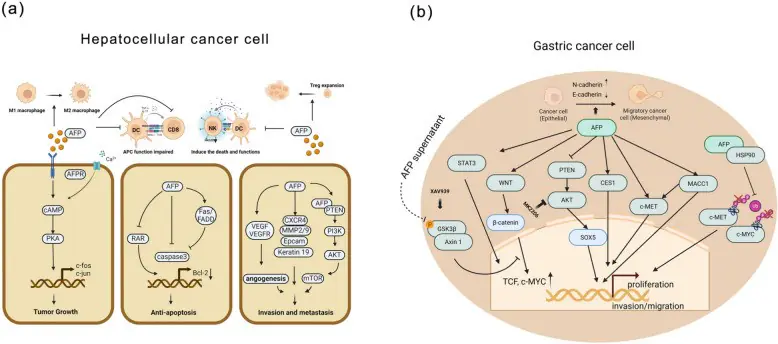
AFP 在肝癌及會製造胎兒甲種蛋白(AFP)的胃癌中的角色。
- AFP 介導的肝細胞癌細胞致癌功能示意圖。AFP 透過 cAMP-PKA-c-fos/c-jun 途徑促進腫瘤生長,透過 RAR-caspase 軸抑制細胞凋亡,並透過上調 VEGF、MMPs、EpCAM 及活化 PI3K/AKT/mTOR 途徑促進侵襲與轉移。AFP 也會透過抑制 APCs、CD8⁺ T 細胞及 NK 細胞活性來損害免疫反應。
- 在會製造胎兒甲種蛋白(AFP)的胃癌細胞中,AFP 透過活化 STAT3、WNT/β-鏈蛋白、c-MET 及 SOX5 途徑,促進增殖、侵襲與遷移,同時抑制如 PTEN 等腫瘤抑制劑。AFP 也透過 HSP90 穩定 c-MYC,並參與上皮-間充質轉移(EMT)。AFP 是 會製造胎兒甲種蛋白(AFP)的胃癌之惡性表型的核心,使其成為有價值的生物標記及有前景的治療目標
會製造胎兒甲種蛋白(AFP)的胃癌的第一個案例研究由 Bourreille 等人於 1970 年報告。值得注意的是,許多研究者目前支持原始理論來解釋胃癌中 AFP 的產生。此理論指出,由於胃組織與肝組織皆起源於胚胎的前腸,存在內在的發育連結。在原發性胃癌進展過程中,細胞分化可能異常,導致特定基因被抑制。這種抑制會導致部分的細胞分化。隨著致癌過程進展,這些被抑制的基因可能被重新活化,使胃癌細胞能表達潛能並會製造胎兒甲種蛋白(AFP)。
此機制為理解會製造胎兒甲種蛋白(AFP)的胃癌形成提供了新穎的觀點。 此外,隨著分子病理學與次世代基因定序(NGS)技術的進步,我們對會製造胎兒甲種蛋白(AFP)的胃癌分子特性與致病機制的理解。有了十足的進步。
在 AFP染色陽性胃癌的診斷中,特別是肝臟轉移病例,有顯著的誤診風險為原發性肝癌或混合型腫瘤的機會。由於會製造胎兒甲種蛋白(AFP)的胃癌病程進展迅速且早期發現困難,大多數患者在晚期才被診斷。
會製造胎兒甲種蛋白(AFP)的胃癌,是一種高度異質的疾病,使得準確分類尤其困難。從治療角度來看,會製造胎兒甲種蛋白(AFP)的胃癌治療上面臨多種挑戰,包括肝臟轉移的快速進展、對化療的敏感度低,以及傳統治療方案療效有限。此外,現行的 TNM 癌症分期系統可能無法精準預測會製造胎兒甲種蛋白(AFP)的胃癌患者的預後。缺乏明確的治療目標也限制了標靶治療的有效性,凸顯了需要更有效的診斷與治療策略。
日本研究者本山提出會製造胎兒甲種蛋白(AFP)的胃癌之組織學分類系統,將其分為四大亞型:肝細胞型、卵黃囊腫瘤樣型、胎胃腸道型及混合型。此分類為會製造胎兒甲種蛋白(AFP)的胃癌的診斷與治療提供了重要的病理基礎。會製造胎兒甲種蛋白(AFP)的胃癌的卵黃囊腫瘤樣亞型與預後最差相關。
在形態學上,會製造胎兒甲種蛋白(AFP)的胃癌通常分為兩種明顯類型:透明細胞型與肝細胞型。另一項研究建議進一步將會製造胎兒甲種蛋白(AFP)的胃癌分為四個亞型:肝樣腺癌、卵黃囊樣腫瘤腺癌、腸母細胞型及常見腺癌。
在診斷實務中,會製造胎兒甲種蛋白(AFP)的胃癌的分類是根據肝細胞分化的組織學形態學,而非血清 AFP的水平。這表示許多患者可能呈現正常的血清 AFP 水平,但仍可以被診斷為會製造胎兒甲種蛋白(AFP)的胃癌。值得注意的是,我們團隊根據血清 AFP 與 CEA 的表現水平,提出進一步的 AFPGC 亞分類,識別出 AFP 與 CEA 雙重陽性特徵的亞群。此亞組患者的預後較僅 AFP 陽性者更差。
研究顯示,會製造胎兒甲種蛋白(AFP)的胃癌大約佔西方國家胃癌病例的 15%。而在包括中國在內的亞洲國家,其發生率介於 1.3%至 6.63%之間。會製造胎兒甲種蛋白(AFP)的胃癌常見於年長男性,且多發生於胃竇。這些腫瘤通常被分類為 Borrmann II 型及 Borrmann III 型晚期胃癌,後者較易發生肝臟及淋巴結轉移。與傳統的胃癌相比,會製造胎兒甲種蛋白(AFP)的胃癌更具侵入性,預後較差。其增殖能力較高,且靜脈及淋巴結的侵襲發生率較高,且遠處轉移伴隨新生血管增多。此外,肝臟轉移在會製造胎兒甲種蛋白(AFP)的胃癌中較為常見,無論是同步轉移還是後時轉移。部分研究報告指出,會製造胎兒甲種蛋白(AFP)的胃癌 的肝臟轉移率可高達 33%至 72%,且肝臟轉移被視為 會製造胎兒甲種蛋白(AFP)的胃癌之獨立且預後不良的因子。
會製造胎兒甲種蛋白(AFP)的胃癌在腫瘤微環境中的免疫抑制情況,會比 會傳統的胃癌更為明顯。沈氏團隊對臨床樣本進行的轉錄組免疫分析顯示,與傳統的胃癌相比,會製造胎兒甲種蛋白(AFP)的胃癌之腫瘤微環境中 CD8⁺ T 細胞、NK 細胞、B 細胞及嗜酸性球的浸潤率顯著降低。相反地,會製造胎兒甲種蛋白(AFP)的胃癌中 CD4⁺ T 細胞的浸潤率顯著較高,顯示免疫狀態偏向為被抑制。另一項研究顯示會製造胎兒甲種蛋白(AFP)的胃癌是一種侵襲性胃癌亞型,特徵為 HLA-G 表現高(71%)、頻繁的 HLA 第一類缺乏症(69%)及低 CD8⁺ T 細胞浸潤,顯示其免疫逃逸機制強健。這些特徵很可能與其胚胎表型有關,暗示腫瘤胎兒的免疫逃逸是惡性腫瘤的關鍵驅動因素,也是免疫治療可以發揮的潛在目標。簡言之,會製造胎兒甲種蛋白(AFP)的胃癌展現出免疫活化降低,導致促腫瘤的免疫微環境。這些特徵顯示免疫檢查點抑制在會製造胎兒甲種蛋白(AFP)的胃癌中可能較為有效,因為會製造胎兒甲種蛋白(AFP)的胃癌其免疫抑制的特性。了解會製造胎兒甲種蛋白(AFP)的胃癌獨特的免疫特性對於設計標靶免疫療法至關重要。我們以 會製造胎兒甲種蛋白(AFP)的胃癌與相關生物標記及免疫細胞的關係作為結論(如下圖)。 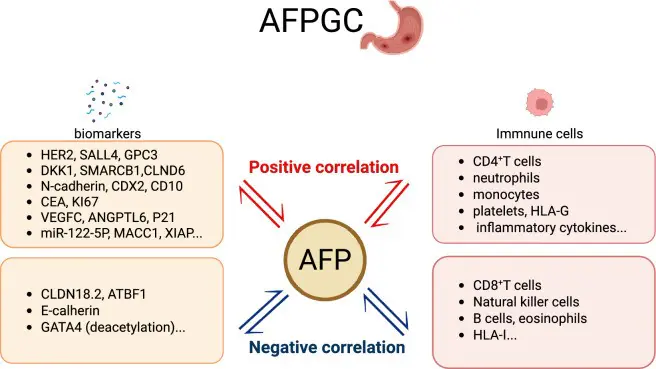
會製造胎兒甲種蛋白(AFP)的胃癌之分子相關的病理特徵。會製造胎兒甲種蛋白(AFP)的胃癌中與 AFP 表現相關的生物標記與免疫細胞族群的簡要摘要。正相關標記包括 HER2、SALL4、GPC3、DKK1、SMARCB1、CLND6、N-cadherin、CDX2、CD10、CEA、KI67、VEGFC、ANGPL6、P21、miR-122-5p、MACC1 及 XIAP 等。AFP 也與 CD4⁺ T 細胞、中性白血球、單核球、血小板、HLA-G 及發炎性細胞激素增加有關。相較之下,負相關特徵包括 CLDN18.2、ATBF1、E-cadherin、GATA4 及免疫成分如 CD8⁺ T 細胞、NK 細胞、B 細胞、嗜酸性粒細胞和 HLA-I,暗示 AFP 在會製造胎兒甲種蛋白(AFP)的胃癌腫瘤進展及免疫逃逸中扮演角色。
早期診斷及根治性手術切除仍是會製造胎兒甲種蛋白(AFP)的胃癌唯一的治癒選項。然而,由於會製造胎兒甲種蛋白(AFP)的胃癌之腫瘤進展迅速且肝臟轉移率高,許多患者在確診時已失去手術機會。即使是接受根治性手術切除的患者,由於會製造胎兒甲種蛋白(AFP)的胃癌具有侵略性,術後復發及轉移的風險仍顯著高於傳統胃癌。不建議符合完全手術切除條件的會製造胎兒甲種蛋白(AFP)的胃癌患者需要接受術前輔助化療。對於早期胃癌(cT1N0M0),內視鏡黏膜切除術(EMR)或內視鏡黏膜下剝離術(ESD)是可行的。然而,由於會製造胎兒甲種蛋白(AFP)的胃癌的早期診斷率較低,且大多數病例在晚期被發現,且會製造胎兒甲種蛋白(AFP)的胃癌的高度惡性表型,即使在腫瘤侷限於黏膜下層的早期病例中,根治性手術後復發率仍偏高。血清 AFP 陽性與淋巴結轉移已被確認為早期胃癌術後復發的獨立風險因子。早期會製造胎兒甲種蛋白(AFP)的胃癌伴隨有腸母細胞分化的研究顯示,EMR 或 ESD 後黏膜下侵襲、淋巴血管侵襲及非治癒性切除腫的機率較高。因此,早期會製造胎兒甲種蛋白(AFP)的胃癌患者需要更密切的監測與追蹤。對於晚期 會製造胎兒甲種蛋白(AFP)的胃癌最佳治療策略是根治手術結合化療,已證明比手術或單純化療有更好的療效,
會製造胎兒甲種蛋白(AFP)的胃癌也可進行經動脈化療栓塞。一項研究顯示,接受經導管化療栓塞的會製造胎兒甲種蛋白(AFP)的胃癌患者存活時間較長,且預後較佳。
由於會製造胎兒甲種蛋白(AFP)的胃癌具有高度侵襲性及惡性潛力,目前尚無標準治療方案。對於錯過手術機會的晚期 會製造胎兒甲種蛋白(AFP)的胃癌 患者,化療是最有效的治療選擇。會製造胎兒甲種蛋白(AFP)的胃癌中化療抗藥性會較製傳統胃癌更為普遍,可能是因為 P-醣蛋白在腫瘤組織中過度表達,導致結果不理想。儘管如此,聯合多藥物之化療仍是主要的治療策略。多項研究建議,無論病期如何,術後都應給予輔助化療。鉑類藥物與其他化療藥物合用,有效的藥物包括氟尿嘧啶、capecitabine、S-1 和irinotecan。雷everolimus是一種 mTORC1 抑制劑,可以提升順鉑化療的療效,並可能作為會製造胎兒甲種蛋白(AFP)的胃癌治療的輔助成分。值得注意的是,儘管順鉑化療扮演的重要角色,Bozkaya 等人在回顧性研究中對改良的 docetaxel、順鉑及 5-氟尿嘧啶(DCF)治療 會製造胎兒甲種蛋白(AFP)的胃癌後,提出了不同的發現。他們的研究結論是,無論 AFP 升高或分泌量如何,這種治療方案對會製造胎兒甲種蛋白(AFP)的胃癌都有效。對於不可切除的 AFPGC,研究顯示 FLEP 方案(5-FU, leucovorin、etoposide及順鉑)可改善預後。臨床上,gemcitabine 已被確認為對會製造胎兒甲種蛋白(AFP)的胃癌是可能有效的藥物。
Ramucirumab 無論單獨治療或與化療合併使用,已被證明對治療會製造胎兒甲種蛋白(AFP)的胃癌是可能有效的標靶藥物。Apatinib治療在晚期 AFPGC 患者中,客觀反應率為 10%,疾病控制率為 70%,無進展存活期(PFS)為 3.5 個月,中位總存活期為 4.5 個月。此外,對於 HER2 陽性 會製造胎兒甲種蛋白(AFP)的胃癌,可選擇針對 HER2 的trastuzumab標靶藥物。先前研究顯示,trastuzumab標靶藥物可與capecitabine及順鉑聯合使用,治療 HER2 陽性的會製造胎兒甲種蛋白(AFP)的胃癌且治療後無復發且存活期超過 3 年。SALL4標靶藥物,如 Entinostat 可透過下調上皮-間充質轉換(EMT)訊號來抑制胃癌細胞的惡性行為,並有效抑制肺癌腫瘤生長。其臨床應用於會製造胎兒甲種蛋白(AFP)的胃癌備受期待,且可能在不久的將來成為現實。
近期研究顯示,AFP 水平較高的會製造胎兒甲種蛋白(AFP)的胃癌者在免疫治療後預後較差,凸顯了量身訂做治療方法的必要性]。然而,一項第一期臨床試驗證明,GLS-010(抗 PD-1 抗體)、lenvatinib 及 XELOX(oxaliplatin 加 capecitabine)的組合,其治療會製造胎兒甲種蛋白(AFP)的胃癌之安全性可接受、且療效令人鼓舞。此外,近期回顧性研究指出,PD-1 檢查點抑制劑與化療結合時,對會製造胎兒甲種蛋白(AFP)的胃癌及肝樣腺癌亞型(患者均有臨床益處。一項第一期臨床研究結果,針對 Lenvatinib 聯合 PD-1 單株抗體及 XELOX 一線治療會製造胎兒甲種蛋白(AFP)的胃癌,顯示疾病控制率達 100%,中位總存活期為 13.17 個月,並取得良好治療效果。許多病例報告也證實,當免疫療法與其他治療結合嫆會製造胎兒甲種蛋白(AFP)的胃癌時,能顯著療效甚至完全緩解。
#會製造胎兒甲種蛋白的胃癌
#胎兒甲種蛋白
#AFP
#肝細胞癌
#卵黃囊腫瘤
#胃癌
#胰臟癌
#膽囊癌
#肺癌
#腸癌
#陳駿逸醫師
#台中市全方位癌症關懷協會
陳駿逸醫師醫療門診服務時段
https://mycancerfree.com/contact/
更多陳駿逸醫師的癌症衛教影片請連接https://www.youtube.com/@mycancerfree
更多腫瘤治療相關資訊 請連接”陳駿逸醫師 與你癌歸於好” https://mycancerfree.com







