文:癌归于好/中西医肿瘤专科 陈骏逸医师
温热治疗(hyperthermia)被定义为利用外源性的热能诱导来应用于治疗,这是一个相当古老而非新鲜的概念,可以追溯到古代,当时热就被用于治疗各种疾病,包括肠胃炎,心脏病、甚至是感冒及恶性肿瘤。
由于各种研究已经证实了温热治疗的潜在分子作用机制,因此在过去的几十年,这种治疗策略变得用于癌症的治疗变得更加流行。
一般而言,温热治疗在结合化疗、免疫、标靶和/或放射线的治疗方案中,被用作为辅助的治疗,化疗或放射线治疗这两种方法,都可以诱导不可逆的癌细胞 DNA 损伤。根据许多体外、体内和临床研究,温热治疗已经被证明也可以通过干扰 DNA 修复反应,来增强 DNA 靶向的癌症治疗策略,偕同增加化疗或放射线的治疗的有益效果。
温热治疗的温度是在 40 到 44°C 之间,它是一种多方面的治疗方式。也是一种有效的放射线治疗的增敏剂,与许多化学治疗剂有良好的相互加乘作用,并且若与放射治疗相结合搭配,可以加强放射治疗的类似“原位肿瘤疫苗接种”的免疫调节效应。
温热治疗在当今的癌症治疗体系何去何从?
简单地说。温热治疗是可以与其他抗癌治疗方法有相互的作用,在化疗、免疫、标靶和/或放射线治疗的方案下,与温热治疗可以互相结合。
温热治疗是一种有效的放射治疗增敏剂
放射治疗可以单独或是与其他治疗方式联合作为治疗癌症的主要方法之一。据估计,45-55% 的新诊断癌症患者都需要放疗,另外 10% 的患者终其一生中是需要再放疗 ,有40% 的癌症治愈是归功于放疗。
放射治疗的主要目的是透过向肿瘤输送杀瘤剂量去诱导癌细胞的 DNA 损伤,同时最大限度地减少对正常组织的剂量。目前放射治疗已经有计划、执行和监测之许多方面的进步,导致了现代的放疗既安全又有效。然而,放疗有一些固有的限制仍然存在,主要如下: (a) 内在 DNA 的修复机制可以防止癌细胞因受到放疗所致的致死损伤转化为亚致死和潜在性致死损伤,从而减少对肿瘤细胞的杀伤; (b) 缺氧的肿瘤细胞存在着对放射治疗的抵抗性; (c) 处于合成期的肿瘤细胞本质上是抗放疗的; (d) 增加放疗剂量虽然可以增强肿瘤控制,但也可能导致急性和晚期正常组织发病的风险更高。因此,目前为改善放射治疗效果而进行的各种不同尝试中,寻找合适的放射增敏剂和辐射调节剂是积极研究的领域之一。
温热治疗已知是最有效的放射治疗增敏剂之一,它结合了诱导肿瘤基质的热生理变化以及细胞与分子水平的持续性之可相互作用
温热治疗与放射治疗相互作用的影响总结如下:
- 1.热疗强化放射治疗:
原则上,热疗强化放射治疗增敏现象对正常组织和肿瘤组织都有影响。
热疗强化放射治疗的增强率取决于癌症组织类型、温度、加热时间以及加热和放射之间的时间间隔。温热治疗的温度越高,加热时间越长,增强作用越大。
当同时进行温热治疗和放射治疗时,热疗强化放射治疗的增强率则是最高,与热疗剂量成比例线性关系,甚至可能达到 5 倍的增强,但它对于肿瘤和正常组织也达到相似的值。因此,同步温热治疗和放射治疗强化前提下,是需要放射治疗精确地勾勒肿瘤的靶点以实现肿瘤的高选择性。随着温热治疗和放射治疗之间的时间间隔增加,无论它们的顺序是如何,热疗强化放射治疗的增强率在肿瘤组织中会下降大约 2 倍,在正常组织中下降大约 1倍。因此,临床上通常是依次序给予温热治疗后再接放射治疗,并且认为温热治疗和放射治疗之间的越短时间的间隔是最佳的,因为它会产生有效和具有肿瘤选择性的放射增敏作用。因为肿瘤选择性的进一步增强,所以肿瘤周围正常组织边缘的温度通常较低。
处于合成期的肿瘤细胞本质上是抗放疗的,但反而是对温热治疗敏感。在>41°C 的温度下,温热治疗还会暂时抑制癌细胞受到放疗所诱导的亚致死和潜在致死 DNA 损伤而进行的修复 。在临床上,放疗诱导的 DNA 损伤得到修复之前,利用温热治疗这种机制,来干扰癌细胞DNA 损伤的修复,是需要提高肿瘤温度与所短温热治疗和放射治疗之间的时间间隔。
温热治疗会藉由诱导 BRCA2蛋白的降解来抑制癌细胞遭受DNA 双链断裂时候所启动的同源重组修复,BRCA2 是同源重组修复的关键。据报导,经典的非同源末端连接 (c-NHEJ) 和替代的非同源末端连接 (alt-NHEJ),其他主要的DNA 双链断裂的修复途径,也部分会受到温热治疗所影响,因为温热治疗会让重要的修复蛋白活性水平降低,包括 Ku、DNA-PK、KU70、KU80 和连接酶 IV。
在没有修复活性的BRCA-2基因缺陷肿瘤细胞中,温热治疗的也被证明还是一种有效的放射治疗增敏剂,表明温热治疗还是会诱导的其他 DNA 修复途径的阻断。由温热治疗产生的 DNA 修复抑制会显著降低肿瘤的 α/β 值,可以优化温热治)。因此,目前在许多临床放疗情况下(包括使用质子疗法),采用放疗大分割策略将大大使得放疗受益于温热治疗的加入。
温热治疗后的生理性血管舒张也可以改善肿瘤灌注和氧合作用,进而促进放射治疗的增敏效应,从而使抗放疗的缺氧细胞转变对放射治疗具敏感性。这种效果需要相对较低、且肿瘤容易达到一定的温度,大约 39°C。临床数据表明,温热治疗会导致部分肿瘤发生再灌流和再充氧,而这种再充氧会让放疗有更好的临床结果。反而是将肿瘤温度升高到 44°C或更高,可能导致肿瘤血管关断,降低肿瘤氧合效应,导致临床放疗结果不良。 .
温热治疗后,氧合效应增强的水平会持续到1-2天。而肿瘤血流的再灌注之发生取决于肿瘤的血管系统以及其对于温度升高的反应之后的血管扩张能力。这种肿瘤特异性会让温热治疗和放射治疗共享时候的强化效应,也让温热治疗和化学治疗同用可以加强肿瘤内的药物递。
- 2.温热治疗具有癌细胞的毒杀性:热能可以通过各种机制杀死癌细胞,包括坏死和细胞凋亡。在缺氧的肿瘤细胞中,在不良微环境和低pH情况下加入温热治疗可以将癌细胞毒杀。因此,温热治疗诱导的细胞毒杀性的效果是温度依赖性,但与温热治疗和放射治疗之间的时间间隔较无关联。因此,温热治疗所诱导的细胞毒杀性将有助于减少放射治疗有抵抗性的癌细胞,并改善临床治疗成绩。
- 3.热治疗的耐受性:温热治疗期间诱导热量,导致随后的温热治疗会使肿瘤组织产生暂时性的抵抗性,从而影响组织对后续温热治疗的热敏感性,这一现象归因于热休克蛋白,其通常于热能压力之后表达会上调。这蛋白质在普遍存在的细胞内部,并且当期释放出来时也可以用于免疫力的调节,涉入对热耐受性的形成。温热治疗后初始肿瘤温度越高,热能恒定持续存在会越长。 临床上,温热治疗采取每周提供一次或两次,用以避免由于过频繁的热能而导致热治疗的耐受性,造成无效的温热治疗。
图1:
临床上的温热治疗其温度达到39-45℃下的多方面之特性作用,其效果是有效的放射治疗的敏化剂; 与化学治疗剂合用有独立,添加和协同作用; 可以做为肿瘤免疫调节剂,是潜在的原位肿瘤疫苗免节剂; 及其具有搭胚有效载荷的磁性纳米粒子的前景。
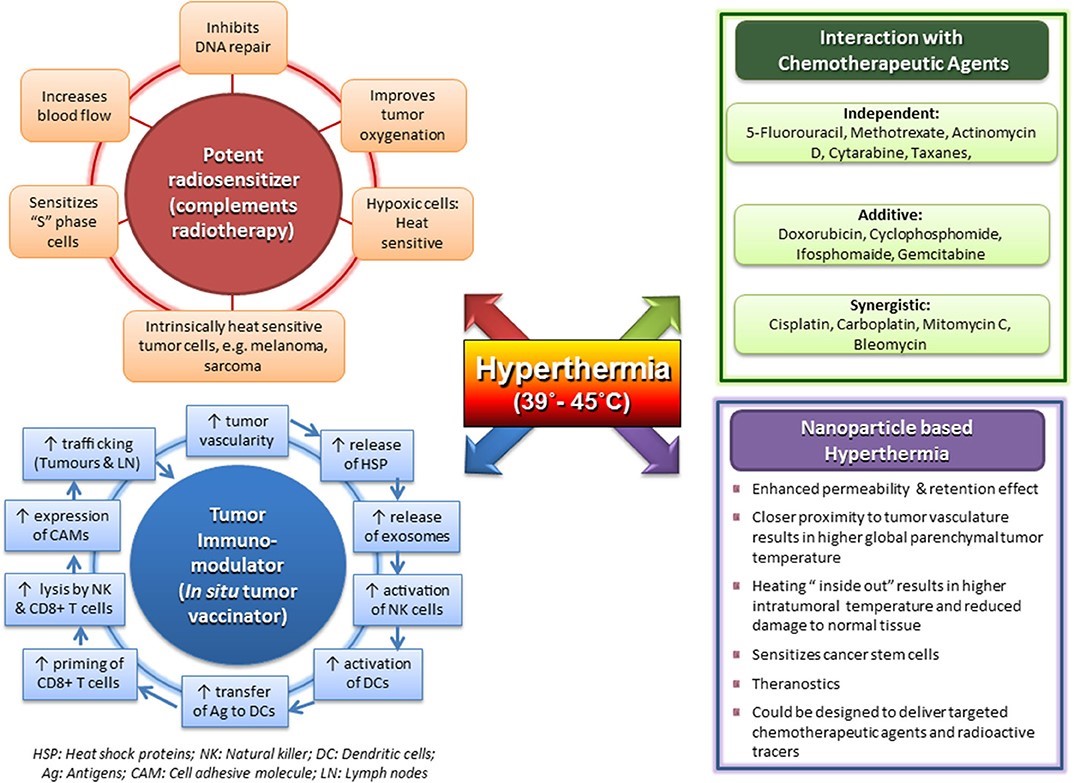
温热治疗是理想的化疗增敏感剂
通过温热治疗改变化疗的细胞毒杀性。体内和体外研究表明,许多化疗药剂在40.5-43℃下表现出细胞毒杀性增强。例如:BCNU、铂金类、Oxaliplatin,和bleomycin。随着温度从37至41.5℃上升,导致细胞毒杀性增强。对于5-氟尿嘧啶(5-FU)mitomycin-C则不明显。顺铂和奥沙利铂显示出超过41-42℃的温度,就会迅速增加细胞毒杀性的倍率值,可能反是热具有诱导干扰DNA损伤的修复的协同作用,类似于与放疗的协同作用。
然而,对于胰脏癌细胞系中的体外研究表明,当给予化疗gemcitabine24小时后进行温热治疗时,化疗的热敏感强化是最佳的。
此外,细胞毒杀性药物会触发靶向药物的递送系统,可以确保更有效的药物递送,避免快速代谢,微脂质体包覆化疗药物是为了增加了其循环的半衰期。微脂质小红莓被设计为利用由于肿瘤的泄漏脉管系统会增强的渗透率和保留效应,让这些药物被动性的积累。然而,已经发现这种被动药物靶向在肿瘤组织内达到的浓度不足。但这可以通过在肿瘤部位的温热治疗让这些高温度敏感的微脂质体触发其释放来改善药物浓度,从而允许更高的局部药物浓度,增加药物渗透,并提高肿瘤内化疗的生物利用度。从而最小化化疗造成的正常组织毒性。
温热治疗更是优质的免疫调节剂
已经证明了39-45°C的温热治疗,可以调节先天和适应性的免疫系统,并于癌症免疫治疗中加入会有协同作用。 温热治疗触发热休克蛋白(HSP),特别是诱导肿瘤细胞释放HSP70的免疫反应。在将肿瘤细胞暴露于较高温度下,蛋白质聚集和变性诱导细胞中压力反应,进行所谓的展开蛋白质反应。因而诱导了Hsp70的水平增加。
因为坏死的细胞失去了膜完整性,所以HSP会充当细胞外的危险信号。 且因为HSP和HSP /肿瘤抗原(AG)复合物都被释放出来,含HSP和含肿瘤的外泌体也从肿瘤细胞排出,如此会激活并吸引树突状细胞(DCS),将其与CD8 + T细胞共刺激,从而通过引发细胞毒杀性T淋巴细胞(CTL),进而诱导T细胞的抗肿瘤免疫。
放疗可以引发免疫抑制和免疫刺激。抗肿瘤的CD8 + T细胞已被证明是放疗所诱导的免疫反应中的关键球员。而温热治疗正可加速放疗的免疫调节过程(图2)。
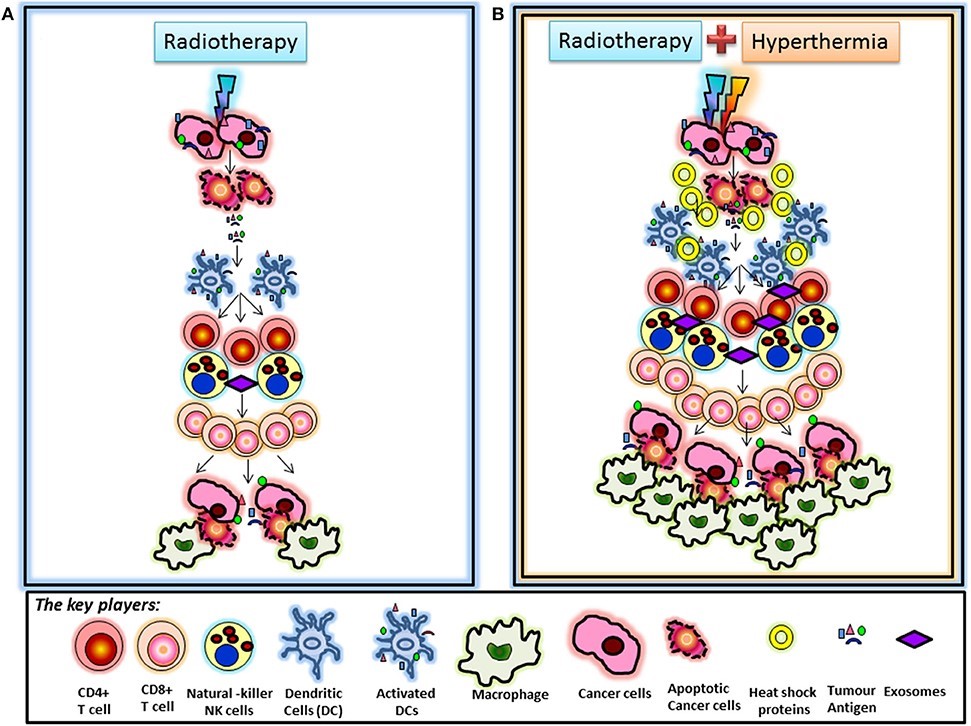
图2:放射治疗与温热治疗诱导的免疫调节:
- 已知放疗通过激活树突状细胞的激活,来介导其后的免疫调节,放射治疗诱导的细胞死亡之后,从癌细胞释放的肿瘤抗原,进而活化的树突细胞后激活T细胞,导致一系列事件,最终导致细胞毒性CD8 + T细胞的刺激。通过放射治疗诱导的趋化因子进一步促进最终通过巨噬细胞清除的肿瘤细胞。
- B.热疗和放疗后的免疫调节:综合热疗+放疗会增加CD68 +巨噬细胞的浸润,加速热疗对免疫调节的结果。众所周知,热疗以及放射疗法通过肿瘤细胞释放热休克蛋白,其可以作为额外的“危险信号”,进一步促进免疫反应。热休克蛋白和含抗原的外泌体可能有助于树突细胞的招募与聚集,导致该部分的免疫调节作用增强。这可能加速放射治疗所诱导的免疫调节。当然这个现象与免疫治疗合并下,更有功效。
温热治疗在临床实务需要整合其他抗癌治疗方式。
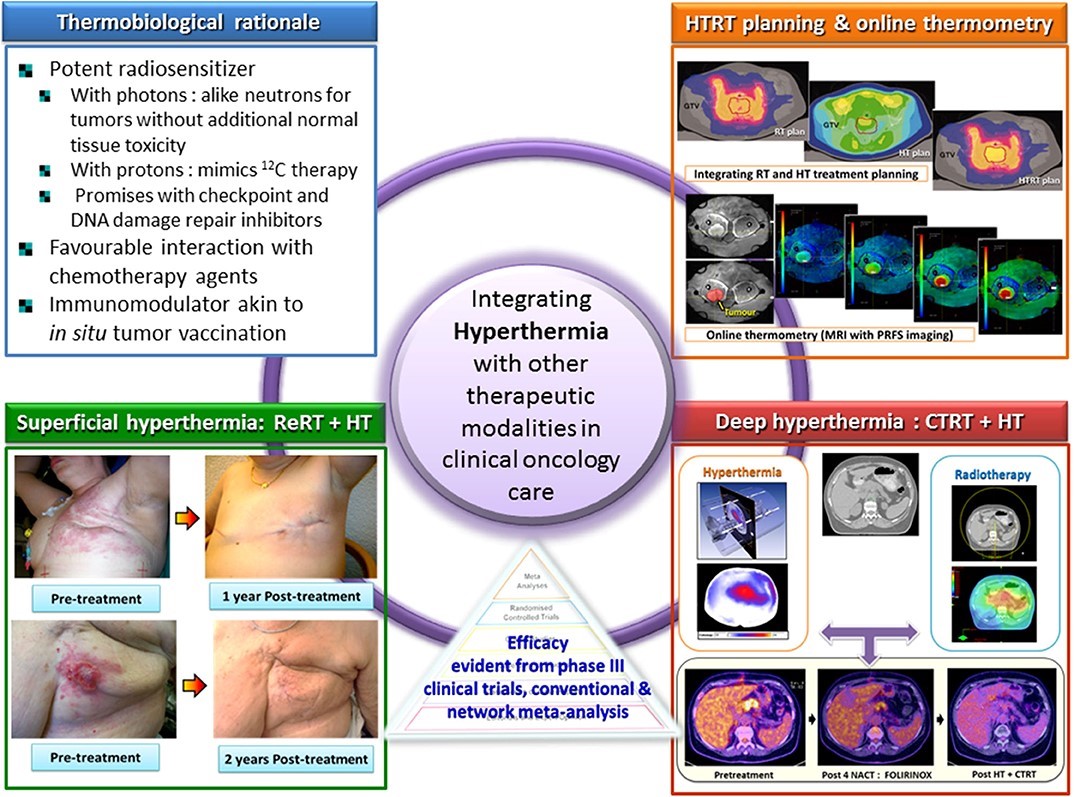
数据源:Front. Oncol., 12 June 2020
#温热治疗
#癌症
#癌症新观点
#话聊俱乐部
#陈骏逸医师
#Hyperthermia
更多陈骏逸医师的癌症卫教影片请连接 https://mycancerfree.com/cn/videos-cn/
更多肿瘤治疗相关信息请连接陈骏逸医师 与你癌归于好https://mycancerfree.com/cn/home-cn/#

