血液腫瘤科/細胞治療中心/台灣細胞免疫醫學會 陳駿逸醫師
腺樣囊性癌是一種源自唾液腺的惡性腫瘤。
自 1859 年 Billroth 首次將其命名為“圓柱瘤”以來,人們逐漸弄清了這種腫瘤的臨床和病理特徵。腺樣囊性癌相對罕見,每年每百萬人中有 3 至 4.5 例,約佔頭頸部所有惡性腫瘤的 1%。該腫瘤主要發生於大唾液腺,其中腮腺和下頜下腺最為常見,約佔所有病例的 37%。其餘病例則發生於小唾液腺以及分佈於各器官組織中的外分泌腺。
腺樣囊性癌常見發生的部位,包括口腔(占比22%)、乳腺(占比17%)、鼻腔和中耳(占比10%),以及肺和支氣管(占比4%)、咽部(占比4%)。此外,也有病例發生在生殖系統、食道及其他解剖部位。
腺樣囊性癌的特徵是生長緩慢,但容易發生神經周圍的侵犯以及局部的復發。部分病例具有較強的侵襲性,會出現遠處轉移,常見的轉移部位,包括:肺、骨和肝臟。臨床表現的多樣性可能與黏液性癌複雜的病理特徵有關。
目前,腺樣囊性癌的病理診斷主要依據三種主要的組織學類型:篩狀型、管狀型和實質型。實質型組織的存在比例被認為會影響患者的預後。
目前,對於腺樣囊性癌的治療方法相當有限,主要為根治性手術切除,手術後通常還會進行輔助性放射治療。化療則是多用於晚期或已發生轉移的病例,但其療效通常有限,所以我們迫切需要能夠有效針對腺樣囊性癌的分子機制的新治療方法。隨著基因檢測技術的發展,人們開始能夠更深入地瞭解腺樣囊性癌腫瘤中的細胞異質性,從而為理解其生物學特性及潛在的治療靶點提供了新的思維。
根據世界衛生組織的共識,腺樣囊性癌是一種由上皮細胞和肌上皮細胞組成的腫瘤。這些細胞會形成不同的結構,而這些結構又會影響預後。篩狀結構的特點是存在由立方形上皮細胞組成的巢狀結構,其中還有充滿糖胺聚糖的囊狀空間;其特徵在於存在鹼性基底細胞。相比之下,管狀結構與最佳的預後是有相關聯,其特點是由基底細胞構成的管狀結構。而實質型結構則會有較差的預後,其特點是基底細胞在緻密的纖維性間質中形成片狀結構;此類結構還與雜合性缺失、染色體異常、體細胞突變以及 p53 蛋白表達升高有關。最近的研究認為,只要腺樣囊性癌存在實質型結構,就應該視為預後不良的指標。.
除了上述三種病理類型之外,腺樣囊性癌還可能出現一種罕見的病理表現,即高級別轉化。高級別轉化的特點是:導管上皮和肌上皮細胞的分化程度很高,細胞有絲分裂活動活躍,Ki-67 指數較高,且 p53 陽性細胞的比例也較高。具有高級別轉化的腺樣囊性癌更具侵略性,局部侵襲和轉移的風險也更高。
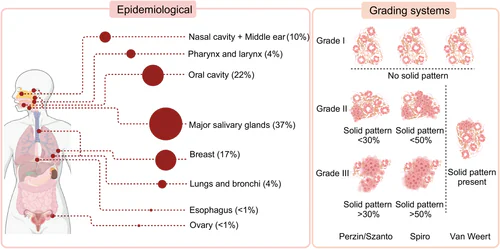
腺樣囊性癌的常見發生部位及病理分級方式。
大唾液腺是腺樣囊性癌最常發生的部位,其次為口腔內的小唾液腺、乳腺以及鼻腔/中耳。
作為腺樣囊性癌的一種特有遺傳學特徵,t(6;9)易位會導致 MYB–NFIB 融合癌基因的產生。這一特徵可作為區分腺樣囊性癌 與其他唾液腺腫瘤的敏感標記。在腺樣囊性癌中,MYB基因的融合起到了驅動基因的作用:它通過 MYC 通路抑制細胞凋亡,同時通過上調 CCND1、下調 p21 來促進細胞週期的進行。此外,MYB 還能通過上調 VEGFA、ICAM1、波形蛋白、N-鈣黏蛋白和α-SMA 來促進血管生成、腫瘤轉移以及腫瘤的間質化過程;同時,它也會調節 API5、BCL2 和 BIRC3 等與細胞凋亡相關的因子。
從機制上來看,MYB 基因轉位所導致的表達增加,可能與所謂的“超增強子”有關。在大多數的腺樣囊性癌病例中,MYB 基因附近都存在有超增強子,這些超增強子提升了 MYB 的表達水平。此外,MYB 蛋白會與那些因轉移而活化的增強子結合,而這些增強子又會與 MYB 的啟動子發生相互作用,從而進一步促進 MYB 的表達,形成正向的反饋循環。另外,腺樣囊性癌中 MYB 的過表達與 3′端非編碼區的缺失有關。通常情況下,MYB 的表達會受到 miR-15a/16 或 miR-150 的抑制。但在腺樣囊性癌的腫瘤細胞中,3′端非編碼區的缺失,破壞了 MYB 與 miRNA 之間的相互作用,從而導致 MYB 基因的過表達。
此外,具有 MYBL1 融合基因的樣本與具有 MYB 融合基因的樣本在基因表達譜上沒有顯著的差異。除了與 MYB 家族的融合之外,一些腺樣囊性癌患者的身上還存在有NFIB 基因的融合現象,例如 NFIB:NFIB 自體融合。不過,這些融合現象對腺樣囊性癌的影響尚不清楚。值得注意的是,我們的分析結果還表明,MYB 基因和 MYBL1 基因的突變或融合是互斥的,這進一步證明了這兩個基因之間的功能冗餘性。這種功能冗餘性源於這兩個基因所擁有的高度同源的 DNA 結合結構域。
值得注意的是,研究指出 MYB 與 MYBL1 融合基因在解剖位置及患者預後方面存在差異。有趣的是,MYBL1 融合基因/過表達的現象多發生在下頜區域。與具有 MYBL1 突變的唾液腺之腺樣囊性癌患者相比,具有 MYB 突變的患者生存期會更短。多變量分析顯示,MYB 的 3′端缺失是影響患者總體生存期的獨立預後標志,且在第三級腫瘤中更為常見(實質型腫瘤中比例超過 30%)。這一看似矛盾的結論可能與 MYBL1 的表達位置有關。Mitani 等人推測,MYBL1 可能在下頜區域的特定細胞中表達;由於該基因位點的排列較為鬆散,因此容易受到 DNA 損傷及修復錯誤的影響。
與在全身各種組織中均表達的 MYB 不同,MYBL1 主要表達於正在發育中的乳腺組織、睪丸生殖細胞、中樞神經系統以及 T 細胞和 B 淋巴細胞中。這種在不同細胞中的差異性表達,或可解釋為何 MYB 和 MYBL1 雖然具有相似的下游作用,但對患者預後的影響卻有所不同。
目前,MYB 不僅被視為一種診斷標記物,同時也是治療腺樣囊性癌的重要靶點。目前,已著手開發MYB 抑制劑來攻擊腺樣囊性癌之腫瘤細胞的臨床試驗正在進行中,這為新藥的開發提供了良好的前景。
作為異二聚體跨膜受體,NOTCH 蛋白在多種細胞的過程中發揮著關鍵作用,包括:細胞分化和增殖,從而維持組織的穩定。NOTCH 受體由跨膜區和細胞外區所組成,它能與鄰近細胞釋放的跨膜配體(如: DLL、Jagged、DLK)可以相互作用。當這些配體與 NOTCH 受體結合後,跨膜區會被蛋白酶給切割,從而釋放出 NOTCH 的細胞內區域(NICD)。
NICD 是一種轉錄因子,它能與 RBPjκ結合,從而調控 HES1 和 REST 等目標基因的表達,進而影響癌細胞的凋亡、上皮間質轉化、細胞遷移和血管生成等各種細胞活動。此外,NICD 還參與了 PI3K–mTORC2–AKT 和 NF-κB 等信號傳導途徑中的基因表達調控。
NOTCH 透過 MAPK 通路參與腺樣囊性癌中的細胞增殖和血管生成,同時也參與細胞間的通信以及導致細胞分化的級聯反應。此外,NOTCH1 的調控失調則可透過調節 MMPs 來誘導 EMT,從而參與腺樣囊性癌之腫瘤的侵襲和轉移過程。
RAS 的錯義突變被視為影響腺樣囊性癌患者的無病生存期和整體生存期的風險因素。TP53 突變與復發性及轉移性腺樣囊性癌患者的整體生存期有相關性,且這些突變與腫瘤的組織學亞型有關,其中在實質性組織學亞型中更為常見。
對於常見的突變,研究人員對 196 名有生存數據的患者進行了生存分析。研究結果表明,NOTCH1(HR = 2.491)和 KDM6A(HR = 3.428)會顯著影響患者的整體生存率。NOTCH1 是一種已被廣泛認可的預後標記物;而 KDM6A 作為一種組蛋白去甲基化酶,參與了超增強子區域 H3K27me1-3 位點的去甲基化過程,可能為腺樣囊性癌的治療提供新的思路。作為 NOTCH 家族最重要的直接下游靶基因,MYC 在腺樣囊性癌的腫瘤發生過程中起著關鍵性的推動作用。NOTCH1–HEY1 通路在腺樣囊性癌中特別活躍,它能促進細胞的間質化轉變以及各種 MMP 家族成員的表達,從而對腺樣囊性癌的腫瘤增殖、侵襲、轉移和凋亡起著重要作用。
總之,NOTCH的訓號通路是腺樣囊性癌的腫瘤細胞分化過程中關鍵的信號;而 MYB 則透過抑制細胞的分化並促進幹細胞增殖,來作為未分化幹細胞的標記。因此,NOTCH1 和 MYB 對腺樣囊性癌細胞的分化具有相反的影響,數據顯示 MYB 家族與 NOTCH1 之間存在互斥的表達模式。研究發現,具有這類突變的患者,其腫瘤發展速度通常更快,且與野生型患者相比,骨轉移和肝轉移等遠處轉移的發生率也更高。
值得注意的是,NOTCH的配體主要在肌上皮細胞中表達,這表明這兩種細胞亞群之間可能存在旁分泌信號傳導機制。此外,MYB 表達水平較高的細胞簇,其與腫瘤侵襲和轉移相關的基因表達也較高,尤其是 NTRK3 基因,該基因屬於神經營養酪氨酸激酶家族。這表明,這些細胞的功能可能與神經通路有關,這與 值得注意的是,NOTCH 配體主要是在肌上皮細胞中表達,這表明這兩種細胞亞群之間可能存在旁分泌信號傳導機制。此外,MYB 表達水平較高的細胞簇,其與腫瘤侵襲和轉移相關的基因表達也較高,尤其是 NTRK3 基因,該基因屬於神經營養酪氨酸激酶家族。這表明,這些細胞的功能可能與神經通路有關,這與腺樣囊性癌的臨床特徵相符,包括其生長能力和對神經組織的侵襲特性。
在 TCGA 研究的 10 條泛癌路徑中,除了 NOTCH、PI3K 和 RTK–RAS 這些已有靶向藥物且腺樣囊性癌癌治療至關重要的路徑外,對 HIPPO–YAP 路徑的研究相對較少。HIPPO–YAP 路徑中的關鍵基因,如 FAT1 和 FAT3,在腺樣囊性癌中常出現突變,而 YAP1 則是腺樣囊性癌中的常見突變位點。
此外,表觀遺傳學上的變化在腺樣囊性癌中也具有非常重要的意義。有研究指出,與染色質重組相關的基因突變,例如:SMARCA4、SMARCB1、SMARCC1、SMARCC2、ARID1 和 PBRM1 等基因的突變,都會導致相關基因的表達下降。在這些突變中,那些編碼 SWI/SNF 染色質重組複合物組成成分的基因的突變尤其重要。這些突變會破壞 SWI/SNF 複合物各組成成分之間的平衡,從而影響染色質的可及性,進而影響下游基因的表達。這種情況可能導致腺樣囊性癌使用化療藥物後的抗藥性。
EGFR 家族通過 PI3K–AKT 或 MEK-ERK訊號路徑,參與了腺樣囊性癌細胞的增殖和遷移過程。在腺樣囊性癌患者中,EGFR 的突變率大約為 1%–2%。大量研究指出,EGFR 過表達與預後不良存在相關性。除了與轉移和增殖相關的機制有關外,研究還表明,EGFR 的活化會通過 c-Myc 誘導 PD-L1 的表達。同時抑制腺樣囊性癌的c-Myc 和 EGFR 信號通路能有效提升治療效果,這表明 c-Myc 可能是 EGFR 通路耐藥性的潛在靶點。
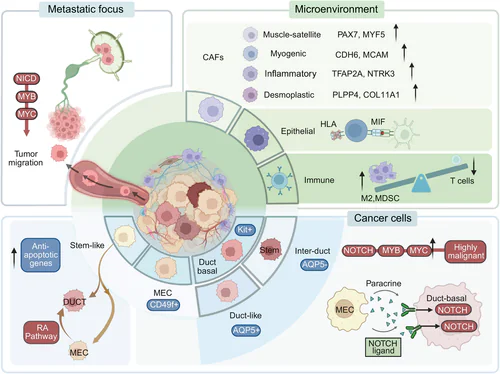
腺樣囊性癌的細胞組成極其複雜。腺樣囊性癌細胞具有明顯的異質性,主要由 MECs 和 DUCTs 組成。MECs會大量表達 NOTCH 配體,與同樣大量表達 NOTCH 受體的 DUCTs 進行旁分泌信號傳遞,從而促進腫瘤細胞的增殖和分化。此外,DUCTs 可進一步分為類管狀細胞和間插型類管狀細胞,後者具有更強的 NOTCH 信號傳遞能力及更高的致癌潛力。
腫瘤微環境中,包含:CAFs、上皮細胞和免疫細胞。CAFs 具有高度異質性,包括肌上皮細胞和肌成纖維細胞等亞群,以及與炎症和結締組織病變相關的亞群,每個亞群都有其特定的分子標記。
上皮細胞的 HLA 表達水平較低,主要通過 MIF 與巨噬細胞或 T 細胞進行交流。腺樣囊性癌之腫瘤的抗原呈現能力和 T 細胞的活化程度均比較低,而 M2 型巨噬細胞和 MDSCs 等免疫抑制細胞的比例則會比較高,從而形成了整體的免疫抑制環境。與原發性病變相比,轉移性病變中 NOTCH 和 MYB 的表達水平明顯更高。在轉移性細胞系中,MYB 通過 NICD 被招募進入細胞內,從而激活 MYC,最終促進腫瘤的遷移。相比之下,淋巴結轉移與原發性病變之間沒有顯著差異。
腺樣囊性癌通常免疫原性較低的。組織學檢查顯示,其淋巴細胞浸潤程度很低,PD-L1 的表達也很少。因此,針對腺樣囊性癌的免疫機制所制定的治療策略相關研究甚少。在 KEYNOTE-028 這項臨床試驗中,共有 26 名患有晚期唾液腺癌的患者參與了試驗,其中 2 名患者患有腺樣囊性癌。這些患者接受了免疫檢查點抑制劑治療,其部分反應率為 12%,應答的中位持續時間為 4 個月。另一項名為 NCT03087019 的臨床試驗則招募了 20 名患有轉移性之腺樣囊性癌的患者。鑒於放射治療能夠增加腺樣囊性癌之腫瘤微環境中 CD8+淋巴細胞和 CD8+/FoxP3+調節性 T 細胞的比例,從而提升對免疫治療的應答效果。
腺樣囊性癌的腫瘤免疫環境具有“冷免疫”特徵,即 T 細胞浸潤程度低、且存在著免疫抑制的作用,這就對現有的免疫療法效果提出了挑戰。在所有藥物治療方法中,抗血管生成療法(如 VEGFR 抑制劑,例如:apatinib 與axitinib)取得了最高的病理反應率,證明其是治療腺樣囊性癌最有效的藥物。
越來越多的證據指出,由於腺樣囊性癌患者之間存在很大的差異性,且腫瘤中的單個細胞也具有多樣性,因此僅依靠一種藥物來治療並不明智。一種有前景的策略是,針對每位患者的特定靶點進行治療,同時再使用抑制相關補償性靶點的藥物。例如,將 NOTCH 抑制劑與 MYC 抑制劑聯合使用;將 AXL 和 MET 抑制劑cabozantinib與 EGFR 抑制劑聯合使用;將 MEK 抑制劑與 p38 抑制劑聯合使用;將 BCL2 抑制劑與 GSIs 或 PRMT5 抑制劑聯合使用。目前有幾項臨床試驗正在進行中,這些或許是克服肺腺癌異質性的最有效方法。
#Adenoid cystic carcinoma
#腺樣囊性癌
#NOTCH
#MYB
#標靶治療
#陳駿逸醫師與你癌歸於好
#陳駿逸醫師
#台中市全方位癌症關懷協會
陳駿逸醫師醫療門診服務時段
https://mycancerfree.com/contact/
更多陳駿逸醫師的癌症衛教影片請連接https://www.youtube.com/@mycancerfree
更多腫瘤治療相關資訊 請連接”陳駿逸醫師 與你癌歸於好” https://mycancerfree.com