血液腫瘤科/細胞治療中心/台灣細胞免疫醫學會 陳駿逸醫師
細胞激素誘導的殺手細胞(CIK細胞)來自週邊血液的單核細胞(PBMC)的體外擴增,並表現出非MHC限制性的細胞毒殺性。
CIK細胞群包括NK樣T細胞(NKT,CD3+ /CD56+)、輔助性T細胞(Th,CD3+/ CD4+/CD56–)、細胞毒性T淋巴球(CTL,CD3+/ CD8+/ CD56–)以及少量自然殺手細胞(NK,CD3–/CD56+)。其體外培養需要IL-2、IFN-γ和抗CD3抗體(OKT3)。
自1991年首次發現並應用以來,CIK細胞已在多種實體癌的臨床研究中得到驗證,顯示出良好的療效和極低的副作用。儘管CIK細胞的製備方法已經較為成熟,但由於供體選擇標準不一致、缺乏標準化的評估方案以及需要符合GMP規範的生產,其更廣泛的應用仍受到限制。總體而言,CIK細胞代表了一種有前景的癌症治療方法。
什麼是 CIK 免疫細胞療法?
您可以把 CIK 細胞 (Cytokine-induced killer cells) 想像成一群送到美國、經過特種訓練的台灣「免疫尖兵」。醫師會抽取病友自身的血液,從病友體內分離出免疫細胞,在實驗室裡「強化培訓」,在實驗室的高標準環境下,加入細胞激素進行(如同教官)進行為期約兩週的強化培訓,讓它們變得更強壯後,讓細胞同時具備 T 細胞的精準偵測能力。之後再回輸CIK 免疫細胞到體內去攻擊癌細胞。將這些訓練有素、數量擴增數十倍的特警部隊回輸到體內。它們會在血液、肝臟及其他器官中持續巡邏,專門清除那些躲過手術與化療、肉眼看不見的微小殘留癌細胞。
病例2的病例介紹
一位85歲男性患者,過去有慢性腎臟病史(病程有8年)、正細胞性貧血病史(病程3年)、高血壓控制良好,以及無症狀性高尿酸血症病史(病程4年),於2023年10月30日因持續性腹脹1個月入院。該患者曾吸菸50包年(5年前戒菸),自述無其他症狀。影像學檢查顯示腹部電腦斷層檢查提示胃竇佔位性病變,懷疑肝門、腹腔、腹膜後及雙側髂窩淋巴結轉移; PET-CT(2023年11月3日;圖3A)證實患者存在全內臟反位、胃竇癌伴廣泛淋巴結轉移(肝門、腹膜後和髂淋巴結)、椎體轉移(C7和T3)以及多灶性肝轉移。
內視鏡切片檢查從胃竇和十二指腸球部取得了6個約1.0 mm的標本。組織病理學檢查(圖3B)顯示為中分化腺癌,其免疫組化特徵符合胃腸道來源,並顯示出提示胃型或胰膽型分化的特徵。
患者拒絕接受全身化療。 11月13日至17日,對C7和T3椎體轉移灶進行了姑息性放射治療(20Gy/5)。 11月19日,患者出現餐後嘔吐未消化食物,臨床表現符合晚期癌症繼發的胃出口阻塞。 11月20日,患者接受了緊急腹腔鏡手術,包括胃空腸吻合術以緩解阻塞,以及切除主要肝臟病灶。
肝臟病灶的組織病理學檢查(圖3C)證實為中分化腺癌伴隨淋巴血管侵犯。免疫組化結果最符合原發性十二指腸或幽門管來源。根據AJCC第八版分期標準,最終分期為TxN+M1(IV期)。
CIK治療開始
患者於2023年11月10日開始接受pembrolizumab(200 mg,第1天/每3週靜脈注射)合併治療,並接受CIK細胞治療,所用細胞為患者兒子的異基因週邊血單核細胞。 2024年4月的系列之全身正子攝影-電腦斷層檢查影像(圖3A)與基線(2023年11月3日)相比,顯示原發性胃竇病灶的體積和代謝活性顯著降低,大部分轉移性淋巴結消退或完全消失,但腸系膜根部出現腫瘤惡化,左側腹股椎溝區和雙側髂血管轉移性發生新的腫瘤惡受累,未檢測到肝轉移。左側腹股溝淋巴結轉移病灶的病理檢查(圖3D)顯示為腺癌,與原發性十二指腸幽門管腫瘤一致。
治療過程中,患者在接受七個療程的pembrolizumab治療後出現免疫相關性肺炎,導致治療於2024年5月9日終止。 CIK療法持續至2024年8月9日,期間順利完成了10次細胞輸注。隨後停止所有抗腫瘤治療,轉為單純支持性治療。
2024年1月,在第三次輸注後,影像學檢查顯示腹部和腹膜後淋巴結明顯縮小(圖3E,2023年10月左圖對比2024年1月右圖)。然而,在停止CIK輸注約4個月後,2024年12月的磁振造影掃描顯示病情惡化,與第九次輸注前後相比(圖3F,2024年6月左圖比較2024年12月右圖)。
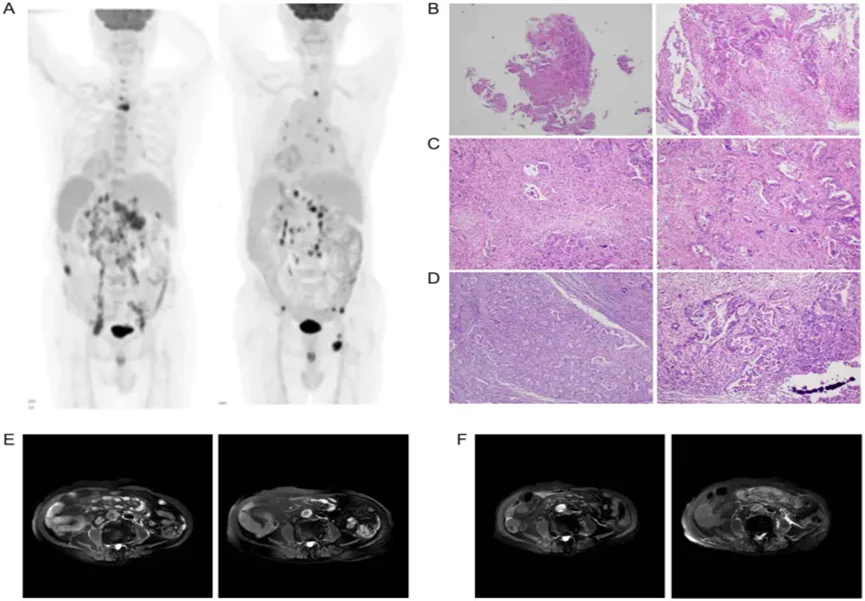
圖3:2024年12月的一系列影像監測顯示病情進展,腹部電腦斷層檢查顯示原發性胃病灶顯著增大。 2025年2月的胸部電腦斷層檢查發現多發性肺部轉移病灶。患者最終死於肺部感染和敗血症等併發症。
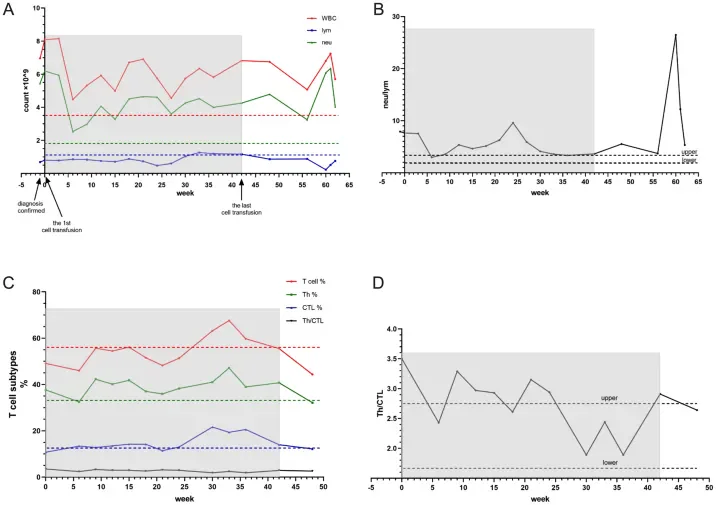
圖4展示了CIK細胞治療過程中監測的代表性實驗室指標,記錄了治療期間的關鍵血液學和免疫學變化趨勢。兩次CIK細胞輸注後,週邊血白血球和嗜中性球計數顯著下降(圖4A),而淋巴球濃度保持穩定。七個輸注的療程後,淋巴球數回升至正常範圍,並維持約10週。停止治療後,淋巴球數再次下降。值得注意的是,淋巴球計數在肺部感染發生時達到最低點(治療停止後約13週),而嗜中性球和嗜中性球/淋巴球比值(NLR)則同時達到高峰(圖4B)。 T細胞亞型顯示Th細胞比例始終高於毒殺性T淋巴細胞(圖4C、D)。
CA 72-4在輸注後迅速下降,隨後在參考值上限附近波動。 CA 125在整個治療期間均低於臨界值,兩種標記在治療停止後均逐漸升高。鐵蛋白水平在治療活躍期升高,與T細胞增加在時間上相關。 CYFRA 21-1和NSE在治療期間在正常值上限附近波動,但在治療停止後會升高。相較之下,SCC和CEA在整個觀察期內保持穩定。
2024年12月,腹部電腦斷層檢查顯示胃部腫瘤惡化。 2025年2月,胸部電腦斷層檢查顯示肺部多發轉移灶。一個月後,患者死於肺部感染和敗血症。
該患者為老年男性,因擔心治療相關不良反應而明確拒絕接受傳統化療。他有吸煙史,在接受免疫治療後出現免疫相關性肺炎。因此,在維持免疫標靶藥物劑量精準調整的情況下,患者開始接受細胞治療。值得注意的是,整個治療過程中,患者對細胞治療方案耐受性良好,未出現治療期間出現的不良事件,睡眠和飲食習慣未受影響,且日常活動水平有所提高。
以下簡要總結了這個病例
病例2為一名老年晚期胃癌患者,因擔心化療的副作用而拒絕接受化療。

病例2是老年男性患者,初診時已廣泛轉移。由於他不適合接受常規的化療,確診後立即啟動了標靶免疫治療。考慮到他高齡且身體虛弱,治療方案中加入了細胞激素誘導的殺傷細胞(CIK)療法。值得注意的是,僅一個療程的CIK細胞輸注後,患者的臨床症狀就得到了顯著改善,足以接受腹腔鏡手術和肝臟病灶切除術,並且觀察到全身病灶顯著縮小。雖然未達到正式的疾病穩定狀態,但患者維持了正常的食慾、睡眠模式和排便/排尿功能,且未出現化療相關毒性反應。在輸注CIK細胞期間,淋巴球數和T細胞亞群均維持在生理範圍內。
CIK細胞回輸後,觀察到白血球和嗜中性球計數均顯著下降,顯示免疫功能恢復,急性發炎減輕。重複CIK細胞回輸後,淋巴球水平升高至正常範圍,並在約10週內保持穩定,之後在治療停止後逐漸下降。值得注意的是,比較分析顯示不同病例間T細胞亞群分佈有顯著差異。這種免疫學差異可能源自以下兩方面:
(1)捐贈者來源的CIK細胞產品中CTL(細胞毒殺性T細胞)/Th組成的固有差異;或
(2)患者特異性因素,包括年齡、基線免疫狀態和腫瘤類型特徵。
值得注意的是,兩種肺癌特異性生物標記物,神經元特異性烯醇化酶(NSE)和細胞角質蛋白19片段(CYFRA21-1),持續處於異常升高的水平,這可能反映了胃腫瘤的雙重上皮起源和神經內分泌分化特徵。新出現的證據表明,CYFRA21-1對胃癌的檢測具有最高的敏感性,而NSE和CA72-4則是預測淋巴結轉移的可靠標記。在此背景下,在CIK治療約30週時觀察到的CA72-4、NSE和CYFRA21-1之腫瘤標記水平的逐漸升高,可能提示疾病早期惡化。儘管鐵蛋白作為腫瘤標記的特異性有限,但其在 CIK 輸注後第 20 週的短暫升高——時間上與 T 細胞擴增高峰期相吻合——可能反映了廣泛的腫瘤細胞凋亡/壞死,隨後細胞內容物釋放入血液循環,之後逐漸恢復正常。
CIK 治療停止後,觀察到免疫功能進行性下降,其特徵是淋巴細胞和 T 細胞計數減少。同時,腫瘤標記開始逐漸升高,直至疾病進展最終導致多重器官衰竭和全身感染。新興的聯合化療治療策略在晚期胃腸道癌症中顯示出增強的抗腫瘤療效。
#CIK
#細胞治療
#體外擴增
#T淋巴細胞
#癌症
#細胞激素誘導殺手細胞
#cytokine-induced killer
#免疫細胞治療
#陳駿逸醫師
#台中市全方位癌症關懷協會
陳駿逸醫師醫療門診服務時段
https://mycancerfree.com/contact/
更多陳駿逸醫師的癌症衛教影片請連接https://www.youtube.com/@mycancerfree
更多腫瘤治療相關資訊 請連接”陳駿逸醫師 與你癌歸於好” https://mycancerfree.com