血液腫瘤科/細胞治療中心/台灣細胞免疫醫學會 陳駿逸醫師
Nectin-4是一種主要在胚胎發育期間表現的細胞黏附蛋白,在健康成人的組織中表現極低,但在多種實體腫瘤中會異常高度表現。這種特性使其成為癌症診斷、預後評估以及近年來作為熱門的癌症治療靶點標靶治療(特別是抗體藥物複合體,ADC)的關鍵標靶。Nectin-4的其表達程度與腫瘤進展、腫瘤侵襲性及較差的預後相關。
Nectin-4 在胚胎階段於人體組織中高度表達,但在健康成人組織中則很少出現。值得注意的是,Nectin-4 可以作為乳癌的組織學或血清學生物標記物,也是乳癌的預後不良的獨立因素。此外,Nectin-4 還與乳癌的生長、血管生成、轉移及復發密切相關。由於Nectin-4 在包括乳癌在內的惡性腫瘤中特異性地高度表達,且Nectin-4 參與了乳癌發展的多個方面。目前已經針對 Nectin-4 開發了多種抗乳癌之標靶治療的策略,針對乳癌中 Nectin-4 的治療之最新研究進展已顯示出令人期待的療效。
而根據癌症基因組圖譜項目的研究,Nectin-4 基因的擴增在多數實體癌症中都很常見。癌症中Nectin-4有過度的表達,計有:
泌尿道上皮癌 (Urothelial Carcinoma):包含膀胱癌,是目前 Nectin-4 標靶藥物應用最成熟的領域,超過 90% 的患者具有Nectin-4有過度的表達。
乳癌 (Breast Cancer):特別是在三陰性乳癌中,Nectin-4 被視為重要的預後生物標記。
非小細胞肺癌:超過 60% 的患者會出現 Nectin-4 過度表現。
其他癌症:包括胰臟癌、卵巢癌、胃癌、食道癌及部分皮膚癌(如黑色素瘤)。
細胞與細胞的黏附指的是相鄰細胞通過細胞黏附分子之間的相互作用,而相互黏附的過程。細胞與細胞的黏附可以調節著多種生物活動,包括細胞間信號傳遞、細胞移動以及組織的生長和發育。相反地,細胞與細胞的黏附過程的異常可能會導致各種疾病,包括神經系統疾病和癌症。
在四種主要的細胞黏附分子(cell adhesion molecules)中,選擇素(selectins)和鈣黏蛋白( cadherins)需要鈣離子才能夠發揮作用,而免疫球蛋白超家族(immunoglobulin superfamily ,簡稱IgSF)和整聯蛋白( integrins)則不需要鈣離子。nectin 屬於免疫球蛋白超家族的亞家族,包含四種成員(Nectin-1 至 Nectin-4),每種成員均是由相應的脊髓灰質炎病毒受體相關基因(poliovirus receptor-related,簡稱PVRL)編碼。其中,位於 1 號染色體 1q23.3 區域的 PVRL4 基因會負責編碼出Nectin-4。與 Nectin-1~3 有不同,Nectin-4 在健康成人組織中較為罕見,但在胚胎和胎盤組織中表達量很高,在外胚層發育和妊娠過程中起著關鍵作用。例如,一種名為ectodermal dysplasia-syndactyly syndrome的體染色體隱性遺傳疾病,正是由於 Nectin-4 的異常表達和功能障礙所導致的。此外,滋養層細胞中 Nectin-4 的過度表達可能引發異常的免疫反應,從而導致先兆子癇。
此外,Nectin-4 也參與了乳房的發育以及泌乳激素信號的傳遞。在懷孕期間,乳腺中泌乳區的形成是需要 Nectin-1 和 Nectin-4兩者共同參與的細胞黏附過程。研究證實,Nectin-4 能與泌乳激素受體相互作用,並促進乳腺泡發育相關基因之β-酪蛋白的轉錄,從而推動乳腺的泌乳功能分化。
Nectin-4可以促進腫瘤的增殖與遷移,也會促進腫瘤新生血管的形成,以及促進腫瘤的上皮間質轉化(EMT)。在癌細胞群中,存在了一類群被稱為癌症幹細胞的細胞,它們具有與健康幹細胞或祖細胞相同的特徵。在某種癌症中觀察到的所有癌細胞類型都源自癌症幹細胞,它們具備自我更新、分化以及形成腫瘤的能力。癌症幹細胞被認為是導致癌症轉移、治療抗藥性和復發的關鍵因素之一。研究表明,除了 EpCAM、CD44、CD133 和 SOX2 等已知標誌物外,Nectin-4 也是癌症幹細胞的另一重要生物標誌物。在乳癌的幹細胞中,Nectin-4 的表達水準顯著升高。多項研究證實,Nectin-4 會藉由PI3K/AKT訊號通路啟動 WNT/β-Catenin的信號傳導,從而調控癌症幹細胞的自我更新和增殖能力。
Nectin-4 能與特定的免疫細胞上的受體相互作用,包括自然 細胞和 T 細胞,從而通過信號傳導途徑去調節對腫瘤細胞的免疫反應。Nectin-4會導致癌細胞產生藥物抗性。在對trastuzumab抗藥的HER-2乳癌細胞中,Nectin-4 能與 ErbB2 變體的獨特 IV 結構域相互作用,增強其二聚化及酪氨酸磷酸化過程,從而有效激活 PI3K-AKT訊號通路啟動,促進乳癌細胞的合成。
總之,Nectin-4 對許多癌症,包括乳癌的發生和生長至關重要,且因其具有特異性的高表達水平,成為一種可靠的生物標記物。此外,Nectin-4 還積極參與腫瘤血管生成、淋巴管生成、癌細胞的遷移和增殖等與腫瘤相關的各種過程,從而體現了其在癌症生物學中的多方面影響(如下圖)。
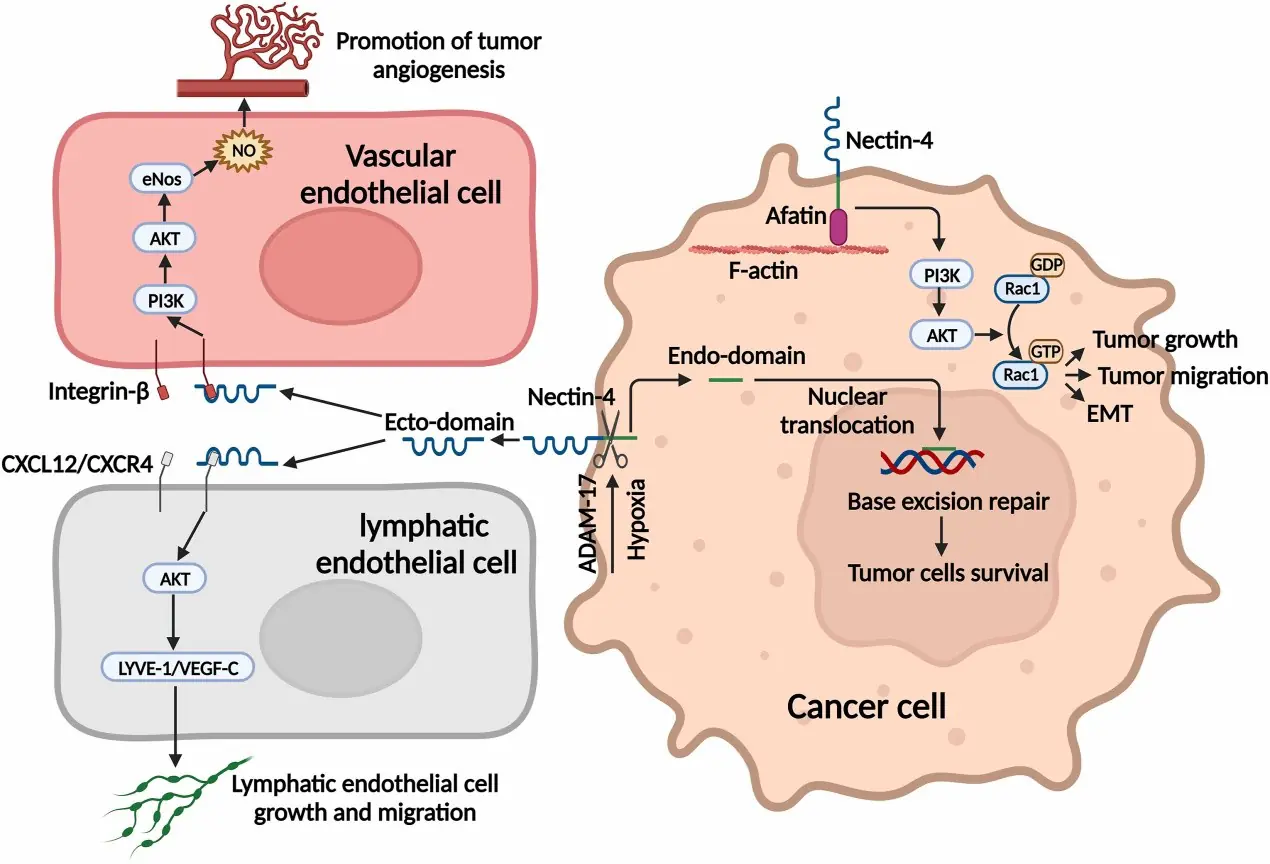
圖:Nectin-4 在癌症中的作用。
Nectin-4 的胞內部分會與 afadin的 PDZ 結構域結合。當表達量上升的 Nectin-4 ,可與 afadin 相互作用,並透過 PI3K/AKT訊號通路進而啟動 Rac1,從而促進癌症的生長、遷移以及上皮-間質轉化(EMT)。
在缺氧條件下,ADAM-17 會特異性地將 Nectin-4 切割為胞外域和胞內域。胞內段會轉移到癌細胞核內,參與 DNA的修復並促進癌細胞的存活。胞外段則與血管內皮細胞的整合素-β結合,通過 PI3K-AKT 訊號通路惠介導的內皮型一氧化氮合酶(eNOS)途徑來促進腫瘤新生血管的生成。此外,胞外段還通過與 CXCR4/CXCL12 相互作用,啟動淋巴內皮受體 1(LYVE-1)介導的淋巴管的生成。
一項收錄 1248 例三陰性乳癌病例的臨床研究結果,顯示Nectin-4 在乳癌組織中具有高表達水準。此外,Nectin-4 mRNA 水平的上升與無癌症轉移生存期縮短有相關,這表明 Nectin-4 具有預測乳癌復發的負面價值。
Enfortumab vedotin (商品名:Padcev / 備思復) 是一種針對 Nectin-4 的抗體藥物複合體 (簡稱ADC),已經獲美德國食品藥物管理局核准用於治療尿路上皮癌。值得注意的是,Nectin-4 也在臨床前和臨床研究中被作為乳癌的治療靶點,故本文會聚焦於Nectin-4 標靶治療策略在乳癌最新研究進展與未來展望。
ADC 由有毒分子與抗體通過化學連接劑共價結合而成,這使其能夠特異性地靶向腫瘤抗原並消滅腫瘤細胞。這些 ADC 能夠識別並結合腫瘤特異性抗原,通過內吞作用形成內體。當細胞內化後,內體會與溶酶體融合,其中的酶會促進細胞毒性分子的釋放(如下圖 A)。此過程通過抑制微管的蛋白、或造成 DNA 損傷來引發細胞凋亡。與單株抗體類似,ADC 中的抗體成分也能通過抑制相應的信號通路(如 PI3K/AKT 訊號通路)來發揮抗腫瘤作用。
此外,ADC 還能與腫瘤微環境中的免疫細胞表面抗原結合,從而刺激抗腫瘤免疫反應。重要的是,ADC 不僅能靶向腫瘤內的抗原陽性細胞,還能消滅抗原陰性細胞。這種特殊的抗腫瘤效應被稱為“旁觀者效應”。當 ADC 被抗原陽性細胞內化並降解後,其釋放的細胞毒性藥物會擴散至抗原陰性細胞,引發細胞死亡。“旁觀者效應”的存在,通常與 ADC 連接器的結構設計以及載藥部分的生化特性有關。值得注意的是,“旁觀者效應”使 ADC 藥物能夠克服抗原表達的異質性,同時保持穩定且有效的抗腫瘤效果。然而,這也可能導致 ADC 藥物偏離預定靶點,從而產生額外的脫靶毒性。
針對 Nectin-4 的治療方法,如ADC、溶瘤病毒(oncolytic viruses)、光熱療法(photothermal therapy)及免疫療法,在早期臨床試驗中均取得了令人振奮的成果。這些療法為將治療手段精確地傳遞給表達 Nectin-4 的癌細胞提供了新策略,從而提升了治療效果並減少了對正常細胞的傷害。
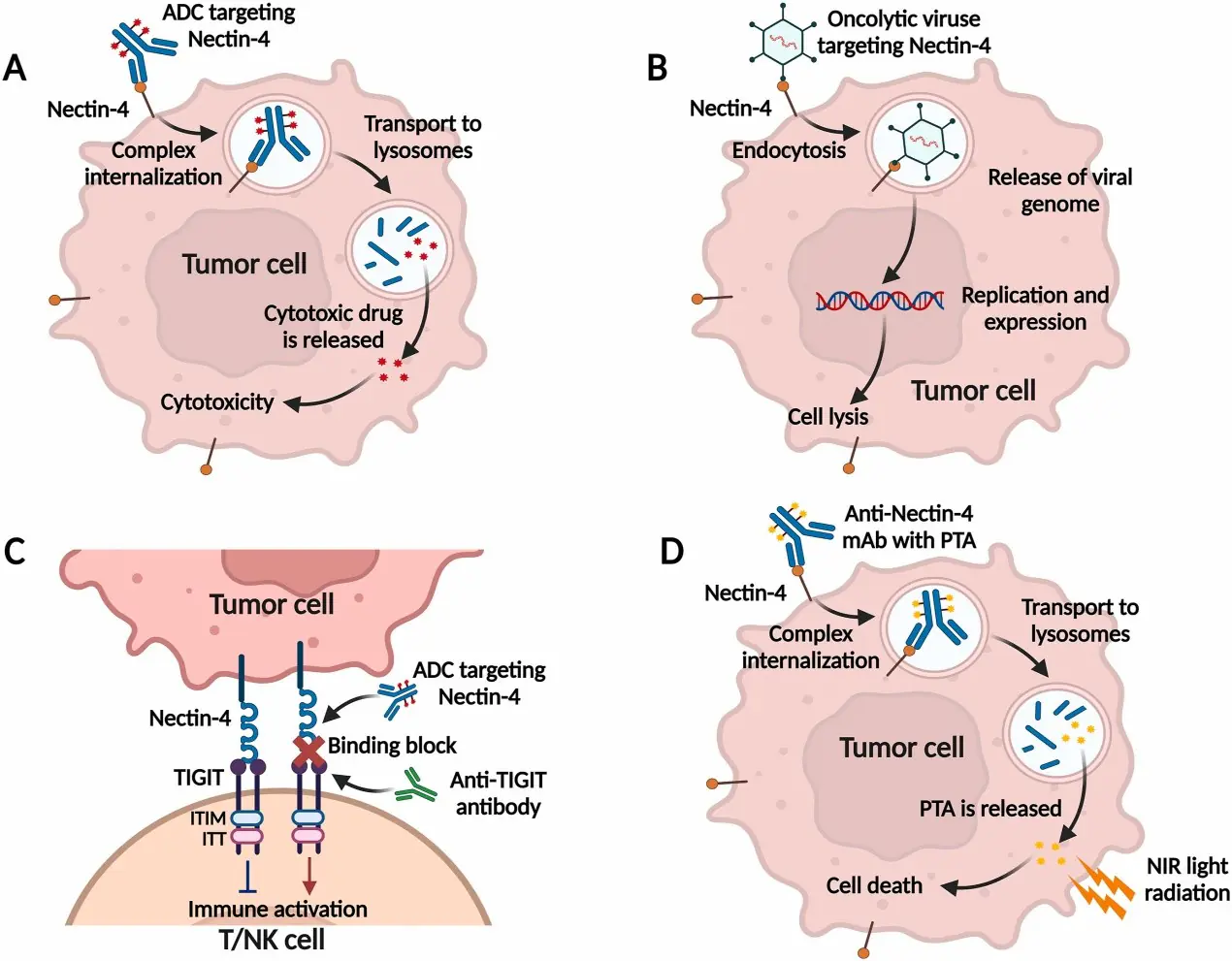
圖 2. 靶向 Nectin-4 的機制。
(A) ADC 與 Nectin-4 結合後被腫瘤細胞內吞,釋放細胞毒性物質,從而導致細胞凋亡。
(B) 靶向 Nectin-4 的溶瘤病毒被腫瘤細胞內吞後,通過複製和表達導致細胞裂解。
(C) TIGIT 與 Nectin-4 的相互作用可通過 ITIM 結構域及類免疫球蛋白酪氨酸尾結構傳遞抑制信號。阻斷 Nectin-4 與 TIGIT 的特異性結合可啟動 T 細胞/NK 細胞。
(D) 靶向 Nectin-4 的光熱療法可將光熱劑送達 Nectin-4 高表達的腫瘤細胞,從而在近紅外光作用下殺死腫瘤細胞。
Enfortumab vedotin (商品名:Padcev / 備思復)能夠靶向 Nectin-4,並通過一種可被蛋白酶切斷的連接基團與單甲基金雀花素 E(MMAE)結合。MMAE 是 dolastatin 10 的合成類似物,通過抑制微管蛋白的組裝來阻礙癌細胞的有絲分裂。體外研究顯示,備思復能夠阻止 Nectin-4 與 Nectin-1 的相互作用,而 Nectin-1 是已知能促進乳癌細胞聚集的因子。在一項臨床前研究中,備思復能以高親和力與 Nectin-4 結合並誘導腫瘤細胞凋亡。此外,體內研究證實,備思復能在多種惡性腫瘤的異種移植模型中誘導腫瘤消退,包括乳癌。備思復的抗癌效果與目標器官中 Nectin-4 的表達水平呈明顯正相關,且具有劑量依賴性。
由於乳癌中 Nectin-4會高度表達,以 Nectin-4 為靶點的 ADC 在此領域具有相當大的治療潛力。備思復能夠有效抑制由 Nectin-4 引發的整聯蛋白β4/SHP-2/c-Src 的活化,從而阻止 Nectin-4 與 Nectin-1 相互作用所促成的癌細胞聚集。備思復能夠有效抑制異種移植模型中的乳癌生長。此外,EV-202 試驗還評估了單藥備思復的治療在三陰性乳癌和荷爾蒙受體陽性乳癌的療效。荷爾蒙受體陽性乳癌的確認客觀反應率為 15.6%,三陰性乳癌為 19%,EV 在兩種乳癌組中均顯示出抗腫瘤活性且副作用可耐受。下圖所示Nectin-4乳癌中的作用:
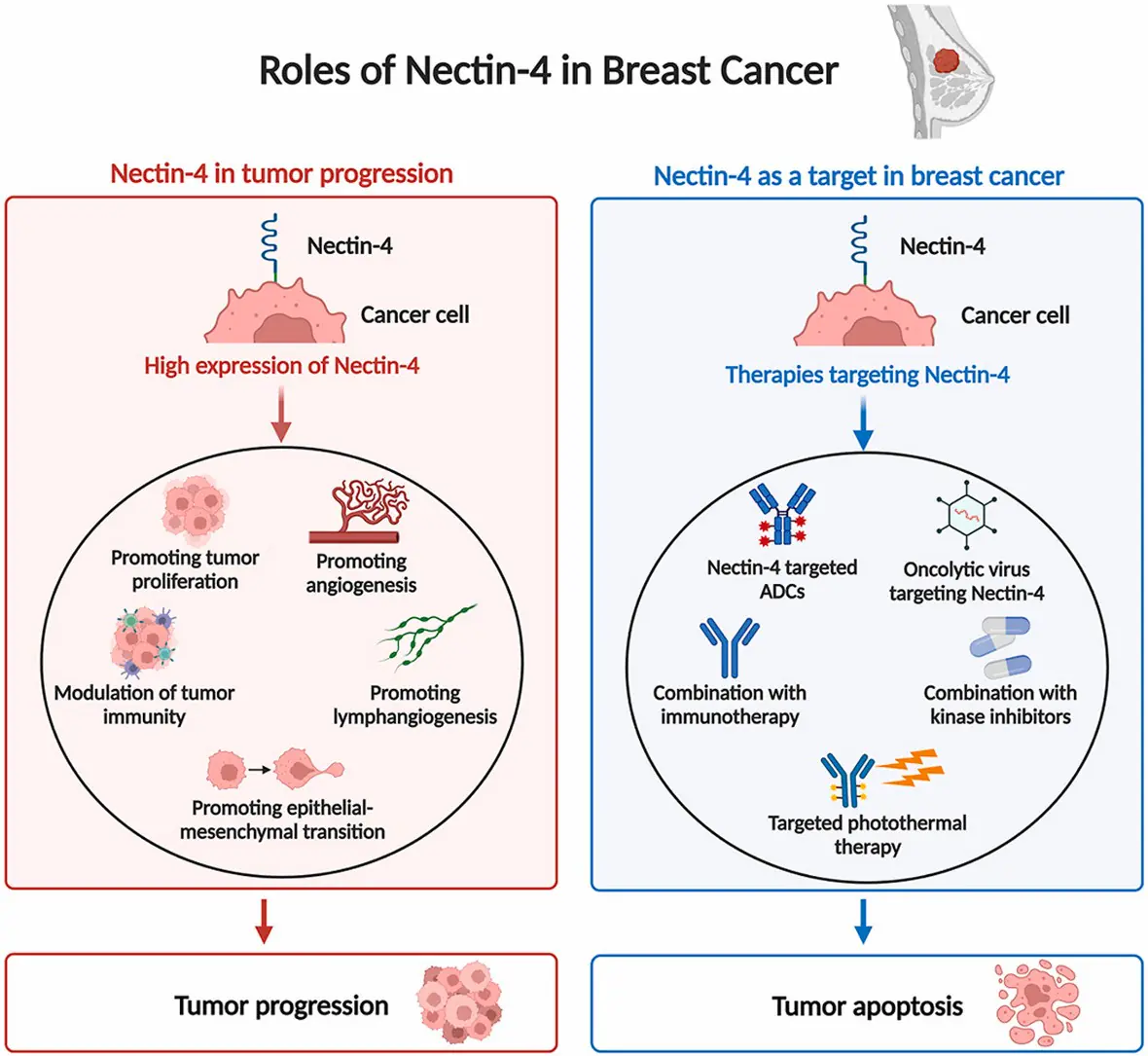
Nectin-4的ADC與其他抗癌治療的結合
Nectin-4 也是免疫檢查點分子 TIGIT 的特異性配體,當阻斷二者之間的相互作用,有望可以增強細胞毒性 T 淋巴細胞和自然殺傷細胞的抗腫瘤效果。綜上所述,將抗 TIGIT 免疫檢查點抑制劑與靶向 Nectin-4 的ADC結合使用,可能會產生協同的抗腫瘤效果。
先前的研究指出,ADC 能夠啟動多種內質網應激反應的通路,從而引發具有免疫原性的腫瘤凋亡,並啟動涉及 T 細胞的免疫反應],這替 ADC 與免疫檢查點抑制劑療法相結合的研究奠定了基礎。EV-303(亦稱為 KEYNOTE-905)是一項重要的第三期臨床試驗,主要研究組合療法對於肌肉侵襲性膀胱癌 (MIBC) 患者的療效。該試驗特別針對那些「不適合」或「拒絕」接受順鉑 (Cisplatin) 化療的高風險患者。評估在手術前後(圍手術期)使用 Padcev (Enfortumab Vedotin) 聯合 Keytruda (Pembrolizumab) 的療效與安全性。將患者隨機分為三組:
組別 A:手術前接受 Keytruda,手術後繼續使用 Keytruda。
組別 B:僅接受手術(根除性膀胱切除術),這是目前的標準治療方案。
組別 C:手術前後均接受 Padcev 與 Keytruda 的組合療法。
與單純手術相比,備思復與免疫檢查點抑制劑的組合療法顯著改善了無事件生存期 (EFS) 和總生存期 (OS)。數據顯示,該療法降低了 60% 的疾病進展或死亡風險,並降低了 50% 的死亡風險。且該試驗達到了第三期研究中史上最高的病理完全緩解率 (pCR)。核准現況:基於此試驗的優異數據,美國 FDA 已於 2025 年 11 月核准此組合療法用於治療該類別患者。
除了免疫檢查點抑制劑之外,備思復與口服標靶藥物Cabozantinib的聯合使用也是重要的研究方向。Cabozantinib是一種多靶點酪氨酸激酶抑制劑,能抑制血管內皮生長因子(VEGF)、間充質上皮轉化因子(MET)以及受體酪氨酸激酶 AXL。早期臨床試驗(NCT04878029)研究了Cabozantinib搭配備思復在轉移性尿路上皮癌中的使用效果。初步研究結果表明,每日 20 毫克Cabozantinib搭配備思復的聯合使用,具有早期的抗腫瘤效果,且安全性良好。此外,對於那些在含鉑化學治療後病情惡化的、具有體細胞 FGFR2/3 突變的轉移性尿路上皮癌者,建議使用成纖維細胞生長因子受體(FGFR)抑制劑Erdafitinib進行治療。
隨著針對Nectin-4的ADC聯合其他抗癌治療策略不斷完善,其在乳癌中的應用也指日可待。尤其是考慮到 EV-202 試驗中備思復的單藥治療在乳癌方面並未達到預期效果。將靶向 Nectin-4 的 ADC 藥物與化療、和爾治療和放射治療等傳統乳癌治療方法聯用,其潛力值得未來進一步研究。
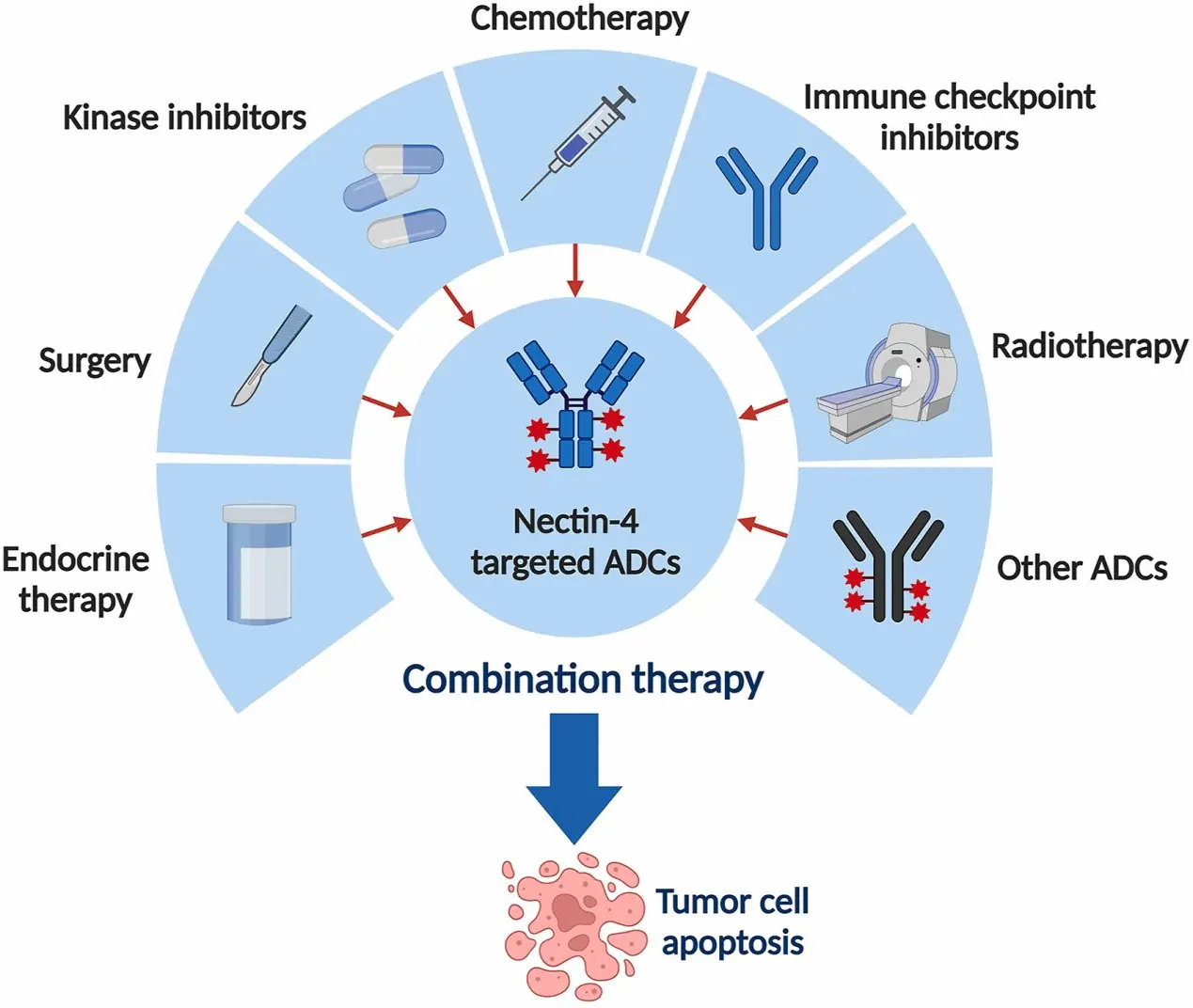
Nectin-4 在乳癌的角色與臨床應用
Nectin-4 在包括乳癌在內的多種癌症中均表現出高度的表達,這一現象引起了癌症研究領域的極大興趣。目前,針對乳癌中 Nectin-4 的療法,如 ADCs,通常將其作為靶點,精準遞送殺傷腫瘤的有效成分。過度表達的 Nectin-4 參與了乳癌發展的多個方面,包括癌細胞的增殖、轉移、血管生成、EMT 過程以及腫瘤免疫微環境。
包括乳癌在內的多種癌症中已知會高度表現Nectin-4細胞黏附蛋白和HER2受體,進而促進癌細胞的生長和擴散。研究人員利用Nectin-4和HER2皆呈陽性的惡性人類乳癌細胞株T47D和SUM190-PT,證實Nectin-4與HER2發生順式交互作用,增強其二聚化與活化,進而活化PI3K-AKT訊號通路,促進癌細胞的DNA合成。 Nectin-4的第三個免疫球蛋白樣結構域與HER2的第四結構域順式連接。此區域與trastuzumab相互作用的區域不同。然而,它存在於trastuzumab抗藥性的ErbB2剪接變異體中,包括p95-ErbB2和ErbB2Ex16。trastuzumab抗藥性的剪接變體也與nectin-4發生順式相互作用,從而增強PI3K-AKT訊號通路,促進癌細胞的DNA合成。
在缺氧條件下,Nectin-4的胞外結構域(此結構域與內皮細胞上的整合素4相互作用)會因為轉移性之乳癌幹細胞介導的ADAM-17表現,而脫落到周圍的基質中。這種結合並非透過磷酸化ERK或NF-α通路,而是透過Src、PI3K、AKT和iNOS路徑刺激腫瘤血管的新生。其在腫瘤血管的新生中的作用已透過體外、卵內和體內血管生成級聯反應的活化和抑制得到證實。因此,破壞nectin-4胞外結構域和整合素-4的連接可能是一種抑制轉移性之乳癌幹細胞所誘導的腫瘤血管的新生的策略。
重組麻疹病毒 rMV-SLAMblind是經過基因改造(通常是在其血球凝集素 H 蛋白引入突變,如 R533A),使其失去了與 SLAM (Signaling Lymphocyte Activation Molecule) 接合的能力。rMV-SLAMblind的主要受體是 Nectin-4 (也稱為 PVRL4 或 Poliovirus receptor-related 4)。研究發現,75%的三陰性乳癌細胞株會在其表面表達出nectin-4,nectin-4是recombinant measles virus (rMV) -SLAMblind的受體。在以rMV-SLAMblind感染後表達nectin-4的三陰性乳癌細胞株進行的體外實驗發現,一半的受試三陰性乳癌細胞株其存活率顯著降低。此外,腫瘤內注射rMV-SLAMblind可抑制MDA-MB-468和HCC70之三陰性乳癌細胞株異種移植的生長。研究人員將表達螢光素酶的rMVSLAMblind靜脈注射到MDA異種移植瘤小鼠體內,以評估標靶治療轉移性乳癌的有效性。病毒在腫瘤內增殖,顯著減緩了腫瘤的生長。病毒會在三陰性乳癌的腫瘤內增殖,顯著地減緩三陰性乳癌的腫瘤的生長。研究人員將病毒靜脈注射到正常食蟹猴體內,檢驗了病毒的安全性;結果未出現任何類似麻疹的症狀。這些發現提示了rMVSLAMblind是治療晚期和/或三陰性乳癌的一種可行的治療選擇。
癌細胞在腫瘤發展的各個階段會暴露在不利的細胞外基質環境中,所以它們必須要適應環境以克服matrix anchorin降解所導致的生長限制。Nectin-4最初是在尋找能夠使細胞分裂不依賴基質錨定的基因時被發現的。 Nectin-4透過促進細胞間黏附和基質非依賴性的integrin 4/SHP-2/c-Src知激活,促進細胞黏附的非依賴性。研究人員發現,Nectin-4是乳癌細胞發育所必需的。此外,透過使用單株抗體阻止Nectin-4驅動的細胞間黏附,研究顯示這種獨特的標靶治療方法可以減緩活體生物體內原位移植腫瘤的生長。
一項研究探討了Nectin-4表現與淋巴結陰性T1/T2期乳癌患者臨床預後的關係。研究納入了197位原發性單側乳癌(T1/T2期)患者,這些患者均無淋巴結的轉移或遠端轉移。研究採用免疫組織化學晶片分析檢測Nectin-4蛋白的表達,並使用Kaplan-Meier存活曲線和多因子Cox回歸分析將結果與臨床數據進行比較。 17.3%患者在細胞膜上表現Nectin-4(m-Nectin-4),而74.8%患者在細胞質中顯著表現Nectin-4(c-Nectin-4High)。 Kaplan-Meier存活分析顯示,m-Nectin-4陽性患者的無疾病存活期(DFS)和遠端復發無惡化存活期(DRFS)都會比較短。根據這項多因素研究,在Luminal A型之荷爾蒙受體陽性的乳癌中,m-Nectin-4陽性是無疾病存活期(DFS)和遠端轉移無惡化存活期(DRFS)的獨立預測因子,但並卻非局部復發無惡化存活期(LRFS)的預測因子。另一方面,在Luminal A型之荷爾蒙受體陽性的乳癌患者中,c-Nectin-4表達者反而有顯著的較長的DFS和LRFS,但與DRFS無關。此多因素研究也表明,因此,該研究提出,在荷爾蒙受體陽性的早期乳癌中,Nectin-4既可作為預後指標,也可作為分子治療的標靶。
另一項研究探討了Nectin-4在Luminal B型之荷爾蒙受體陽性、HER2陰性乳癌中的表現。該研究納入了原發性單側乳癌且無轉移跡象的患者。以免疫組織化學方法檢測nectin-4蛋白的表達,並使用Kaplan-Meier存活曲線、多因子和單因子逐步比例風險分析將結果與臨床數據進行比較。 Nectin-4過度表達與總存活期、無疾病存活期和遠端無復發生存期呈負相關,其相關性與腫瘤大小的相關性相同。
一些研究證實Nectin-4會參與淋巴管生成並調控浸潤性乳管癌的淋巴管生成。飲酒、吸菸、不健康的生活方式以及其他乳癌危險因子,以及CXCR4的表達和淋巴管密度均與nectin-4表達呈現正相關。Nectin-4 透過調控 CXCR4/CXCL12-LYVE-1 軸,在驅動腫瘤誘導的淋巴管生成和淋巴轉移中發揮了重要作用。
Zelenectide pevedotin(原名 BT8009)是一種高度選擇性的Bicycle Toxin Conjugates® (簡稱BTCs) 是一種新型的標靶抗癌藥物,由 Bicycle Therapeutics 開發。它們被設計用來克服傳統抗體藥物複合體 (ADCs) 的侷限性。該藥物由一種針對 Nectin-4 的雙環肽與MMAE 偶聯而成。與ADC聯物相比,BTC®分子的分子量更小、血漿半衰期更短,且具有獨特的藥代動力學特性,即能夠快速滲透腫瘤組織,同時將對健康組織的損害降至最低。在一項包含 245 名乳癌患者的大型獨立研究中,NECTIN4基因擴增的出現率分別為:荷爾蒙受體陽性乳癌患者中的 19%、HER2受體陽性乳癌患者中的 14%以、三陰性乳癌患者中的 23%。
有 32 名重度治療的三陰性乳癌 患者加入Zelenectide pevedotin 的單藥治療劑量遞增和擴展組研究。 共有 31 名三陰性乳癌患者接受了Zelenectide pevedotin的 2 期臨床試驗推薦劑量,既往治療線數中位值為 6 種,ECOG 評分為 0 或 1 的分別占 50.0%。在 32 名接受Zelenectide pevedotin治療的患者的其中,Zelenectide pevedotin治療的總緩解率為 13.3%。19 名患者接受了 NECTIN4 檢測,其中 6 名呈陽性(31.6%)。在這些陽性患者中,3 名接受Zelenectide pevedotin治療的患者達到腫瘤部分緩解,總緩解率為 50.0%;其餘 3 名患者的病情保持穩定(病情控制率為 100.0%),所有NECTIN4 檢測呈陽性的患者,此前都接受過sacituzumab govitecan.治療。在 NECTIN4 檢測呈陰性的 13 名患者中,有 1 名達到部分緩解:總緩解率為 7.0%。7%(95% CI:0.2, 36.0)。NECTIN4 擴增似乎具有臨床預測價值,可幫助識別那些對 Zelenectide pevedotin 反應更好的三陰性乳癌患者。研究結果支持進一步探索 zelenectide pevedotin 在乳癌患者,尤其是轉移性三陰性乳癌患者中的應用前景及相關分層治療策略。
Nectin-4 在癌症發展中的作用可能為抗腫瘤藥物的研發提供新的思路。例如,Cyclin D1 通過促使細胞週期從 G1 期進入 S 期來促進細胞增殖,它在多種腫瘤類型中均存在過度表達。抑制 Nectin-4 的表達可增加 Cyclin D1 的平準,進而導致腫瘤細胞凋亡。因此,將細胞週期抑制劑與抗 Nectin-4 藥物聯合使用,可能是一種很有前景的抗癌策略。此外,Nectin-4 參與了血管生成的調節,其過表達會導致 VEGF 表達下降、VEGFR2 表達上升,也暗示Nectin-4 療法與抗血管生成療法之間有合作的空間。
#Padcev
#備思復
#抗體藥物複合體
#ADC),
#Nectin-4
#Enfortumab vedotin
#EV
#尿路上皮癌
#乳癌
#三陰性乳癌
#荷爾蒙受體陽性乳癌
#轉移性尿路上皮癌
#Zelenectide pevedotin
#BT8009
#Bicycle Toxin Conjugates
#BTCs
#陳駿逸醫師
#台中市全方位癌症關懷協會
陳駿逸醫師醫療門診服務時段
https://mycancerfree.com/contact/
更多陳駿逸醫師的癌症衛教影片請連接https://www.youtube.com/@mycancerfree
更多腫瘤治療相關資訊 請連接”陳駿逸醫師 與你癌歸於好” https://mycancerfree.com