血液腫瘤科/細胞治療中心/台灣細胞免疫醫學會 陳駿逸醫師
KRAS基因突變發生於超過三分之一的大腸直腸癌,主要影響密碼子 12 和 13,較少見於密碼子 61、117 和 146。其他密碼子中也曾有罕見突變的病例報告,但通常缺乏明確的功能意義。這些突變會啟動驅動細胞增殖、抑制分化並抑制細胞凋亡的途徑。KRAS 突變大腸直腸癌與預後較差、復發率較高、化療反應降低,及對 EGFR 標靶治療的抗藥性有關。KRAS Q61H這是 KRAS 基因第 61 號密碼子的活化突變。與常見的 KRAS G12 或KRAS G13 突變類似,它會導致 MAPK 信號通路持續激活。在大腸癌中,這通常預示著對抗 EGFR 單株抗體(如 Cetuximab 或 Panitumumab)具有抗藥性。
依據大腸直腸癌患者 的KRAS 突變狀態進行分流,現已成為治療指導標準,儘管並非所有突變都具有相同的致癌性或治療反應。過去被視為無法被證實的抑制劑,大多數大腸直腸癌是由控制細胞分裂的基因突變引發的連續過程,導致無法控制的增殖及良性息肉的形成。這些病灶可透過獲得額外的基因組變異,包括染色體異常、基因突變,以及調控增殖、分化、凋亡和血管新生的基因的表觀遺傳修飾而進展為惡性
位於 KRAS基因的第 61 號密碼子(Q61),這類突變會使 KRAS 蛋白因而喪失內源性 GTP 水解能力,使其持續處於「開啟」狀態,導致 RAS 蛋白持續處於活化狀態,進而驅動下游細胞增殖。MAP2K1 p.E203K 的基因彙編碼 MEK1 蛋白,當E203K 是一種「激發性突變」(gain-of-function),會導致 MEK 蛋白不需要依賴上游訊號的啟動、而就能自主性地活化。
當KRAS p.Q61H (密碼子 61 突變)與 MAP2K1 p.E203K這兩種突變同時存在時,通常預示著腫瘤對 MAPK 訊息傳遞通路(Ras-Raf-MEK-ERK)具有高度的依賴性,因為KRAS 位於 MEK(MAP2K1)的上游。當兩者同時突變時,MAPK 通路會受到「雙重打擊」式的活化,這往往與大腸直腸癌更具侵略性的腫瘤行為相關。這種組合可能導致腫瘤對單一標靶藥物(例如僅使用單一 MEK 抑制劑)較快產生獲得性抗藥性,因為下游突變可以繞過上游抑制。
由於當KRAS p.Q61H 與 MAP2K1 p.E203K這兩種突變同時存在時,其對訊息傳遞通路(Ras-Raf-MEK-ERK)的依賴性,所以使用MEK 抑制劑(如: Trametinib)單藥有反應或是聯合使用作潛在的策略。
Ras 蛋白是小型的 GTPase,作為分子開關,啟動調控細胞生長、分化及凋亡的基本訊號轉導路徑。人類擁有三個 RAS 基因——HRAS、KRAS 和 NRAS, 編碼四個蛋白質(KRAS 編碼兩個剪接變異,KRAS4A 和 KRAS4B),序列相似度高。儘管如此,RAS 同型在組織分布、膜定位及下游訊號偏好上存在有差異,導致不同癌症類型中其突變光譜與致癌角色各異。
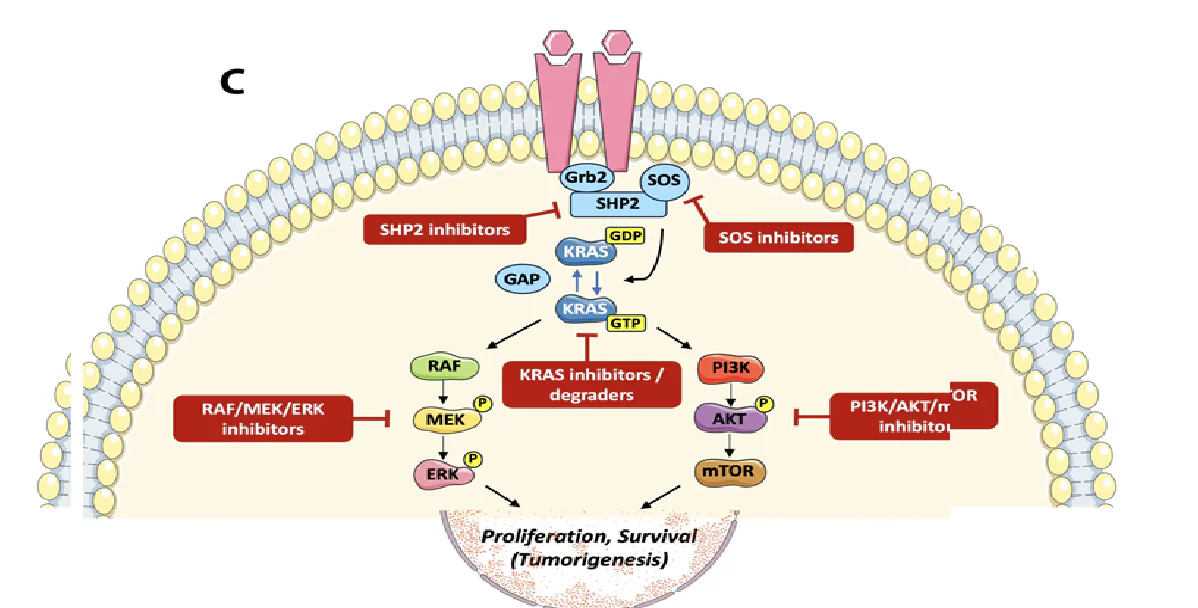
RAS 蛋白會在有活性時會在結合 GTP 的狀態與非活性的結合 GDP 狀態間循環。活化發生在生長因子與膜結合的受體互動時,透過 GRB2 和 SOS(一種鳥嘌呤交換因子 GEF)進行訊號的轉導,這些因子催化 GDP-GTP 交換並活化 Ras。這種構象的變化是由 Ras 效應因子所偵測,啟動下游路徑,最顯著的是 RAF/MEK/ERK(MAPK 途徑)及 PI3K/AKT/mTOR(PI3K 途徑),調控凋亡抑制、細胞生長、轉化、遷移及分化。Ras 是透過 GTP 水解成 GDP 而失活,這過程由 Ras 本身的 GTP 酶活性催化,並由 GTP 酶活化蛋白(GAPs)加速。最顯著的 RAS 缺口是神經纖維素 1(NF1)和 RASA1(亦稱 p120GAP)。
突變的頻率與特徵因癌症類型及 RAS 基因而有所不同,顯示並非所有 RAS 基因突變皆相同,且特定RAS 基因突變展現出獨特的生物學與臨床行為。驅動 RAS 基因中的特定突變主導其他突變的力量,是多重因素的複雜相互作用所成,包括組織特異性因素如基因毒性壓力、生物選擇、基因組拓撲、基因表現及細胞情境。
最常見的癌症相關 Ras的改變是誤義突變,破壞非活性與活躍型態的平衡,通常涉及胺基酸取代,降低 GTP 水解或增加 GTP 負載。
密碼子 12、13、61 及 146 的突變會破壞 GAP所誘導的 GTP 水解,導致持續Ras的活化及持續後續之下游的訊號傳遞,促進細胞存活與失控增殖。
突變胺基酸決定了突變體 KRAS9 的生化活性及轉化能力。攜帶不同 KRAS 突變的細胞在糖酵解、谷氨醯胺使用量以及胺基酸、膽鹼和核苷酸己胺代謝方面也存在有差異,可能影響抗癌治療的反應。
針對 KRAS 上下游的MAPK 與 PI3K 途徑蛋白質的抑制劑,早已獲准臨床應用。然而,開發特定 KRAS標靶藥物面臨了重大挑戰,原因包括 KRAS 對 GTP/GDP 的親和力、高細胞內 GTP 濃度、缺乏變構調控位點,以及 GEF、GAPs 與效應子透過延伸蛋白-蛋白質交互作用,表面形成的複雜交互作用網絡。。此外,GTP 結合口袋在不同 KRAS 突變間有所不同,使抑制劑設計更加複雜。由於直接與間接方法屢次失敗,KRAS 長期以來被視為「無法出藥」。
KRAS G12C標靶藥物在含有 G12C 突變的癌症中有一定成績,但由於其專為KRAS G12C此等位基因設計,對較常見的 KRAS 突變如 G12D 和 G12V 並不具活性。
KRAS Q61H突變會在胰臟腺癌及大腸直腸癌、肺腺癌患者出現,KRAS Q61H 突變會有較具侵擊性的臨床行為、早期轉移擴散及較差的結局。在胰臟腺癌及大腸直腸癌,KRAS Q61H突變會與腹膜及漿膜擴散有密切相關,常伴有腹水及臨床快速惡化。在分子層面,KRAS Q61H 展現出與多種腺癌類型中密碼子 12 變異的生化特性。密碼子 61 突變對內在 GTP 水解的影響比大多數密碼子 12 的置換更為深刻。因此,即使缺乏上游受體酪氨酸激酶輸入,KRAS Q61H 仍能持續活性,此特性使其與許多其他 KRAS 等位基因有所區別。
KRAS p.Q61H 是一種發生在 KRAS 基因之第 3 外顯子(exon 3)第 61 號密碼子的罕見突變,常見於大腸直腸癌。與其他常見的 KRAS 突變(如 G12, G13)類似,p.Q61H 突變會導致 KRAS 蛋白持續處於活化狀態。研究證實此突變會使大腸癌患者對抗 EGFR 單株抗體藥物(如 :Cetuximab 或 Panitumumab)會產生抗藥性。此突變也會使 KRAS 蛋白脫離上游調節,並使癌細胞對 SHP2 抑制劑產生抗藥性。
KRAS Q61H 在腺癌中的一個顯著特徵是其會與 TP53 突變的頻繁共同出現。在肺腺癌中,TP53 是 KRAS Q61H 腫瘤中最常見的共突變基因之一,這一模式與胰臟癌密切相似,後者 KRAS 與 TP53 的共突變,
KRAS Q61H是一種特別具侵略性的分子亞型;實驗模型顯示,TP53 的喪失與 KRAS Q61H突變共同存在,會誘導出基因組不穩定、上皮-間充質轉換及轉移能力,特別是對腹膜等漿膜表面的轉移。
針對KRAS Q61H突變之目標性方法的尋找,深受KRAS Q61H突變之獨特的生物學所影響。鑑於對 MAPK 訊號的優先依賴,MEK 與 RAF的標靶藥物是合理的治療策略。而抑制SHP2的標靶藥物在KRAS Q61H突變上似乎較不具吸引力,由於此等位基因相對獨立於上游的訊號傳導,SHP2 阻斷無法達到 KRAS Q61H 驅動模型中觀察到的路徑的抑制。儘管如此,結合 SHP2 抑制劑與 MAPK 途徑阻斷的組合方案仍在研究中,而此類方法是否能克服 KRAS Q61H突變的初級抗藥性仍是未知數。
KRAS的標靶藥物與 RAS-ON 抑制劑的開發。這些藥物能結合活性 KRAS,不論密碼子為何,現已進入早期臨床試驗,並已在多種 RAS 突變癌症中展現出令人鼓舞的結果。
#KRAS
#Q61H
#基因突變
#大腸直腸癌
#基因檢測
#MEK
#RAF
#標靶藥物
#SHP2
#陳駿逸醫師
#台中市全方位癌症關懷協會
陳駿逸醫師醫療門診服務時段
https://mycancerfree.com/contact/
更多陳駿逸醫師的癌症衛教影片請連接https://www.youtube.com/@mycancerfree
更多腫瘤治療相關資訊 請連接”陳駿逸醫師 與你癌歸於好” https://mycancerfree.com

