血液腫瘤科/細胞治療中心/台灣細胞免疫醫學會 陳駿逸醫師
在下圖中展示了三種不同的免疫編輯正常化的策略,免疫微環境所發生的變化,以便讀者更清楚地瞭解各種正常化策略相結合的優點。三種癌症免疫編輯的治療策略,分別是腫瘤細胞的正常化、免疫系統的正常化以及間質細胞的正常化。
這三種免疫編輯正常化的策略可以同時使用,也可以依序應用,以最大限度地抑制腫瘤的進展並延長患者的生存期。例如,在進行抗種劉血管新生治療後,微環境中具有殺傷腫瘤作用的 T 細胞數量會增加;而在 IFN-γ的作用下,腫瘤細胞和間質細胞上免疫抑制性受體的表達量也會上升。上述微環境的改變,為免疫檢查點抑制劑治療的應用奠定了基礎。抗血管生成治療與免疫檢查點抑制劑治療相結合的可行性已經在臨床上得到證實。
在IMpower150 試驗是一項第三階段的臨床研究,該研究證明瞭在轉移性非鱗狀非小細胞肺癌的一線治療中,將免疫檢查點抑制劑與抗血管生成治療相結合的使用方式,確實能夠改善患者的無進展生存期和整體生存期。在 IMpower150 研究的最終分析中,與單獨使用抗血管生成治療和卡鉑類藥物相比,同時使用atezolizumab、bevacizumab、卡鉑類藥物和紫杉醇的治療組,其整體生存期的中位數有所延長(19.5 個月對比 14.7 個月)。
不過,在應用免疫檢查點抑制劑治療之後,部分腫瘤細胞會失去對於IFN-γ的反應,同時 MHC-I 的表達也會減少。這就使得腫瘤細胞無法被具有細胞毒殺性的 CD8+ T 細胞所識別和殺死。在這種情況下,採用“腫瘤細胞正常化”策略,可以有效地恢復腫瘤細胞上的 MHC-I 表達,進而提升免疫檢查點抑制劑治療的效果。例如,使用表觀遺傳學藥物中的 HDAC 抑制劑,在促進體內腫瘤新抗原的免疫應答,以及增強抗腫瘤免疫反應方面,都取得了令人鼓舞的成果。在一項臨床試驗中,HDAC 抑制劑 entinostat 被用於治療那些對先前的抗 PD-1/PD-L1 免疫治療無反應的晚期非小細胞肺癌患者。結果顯示,entinostat 與抗PD-1免疫檢查點抑制劑 pembrolizumab 合併使用時,能夠產生強效的抗腫瘤效果:有 9%的患者出現了客觀反應。
上述例子說明了各種免疫編輯正常化相結合所帶來的巨大潛力。基於此,我們在上圖中展示了在三種不同正常化策略下,免疫微環境所發生的變化,以便讀者更清楚地瞭解各種正常化策略相結合的優點。
在免疫編輯正常化的治療過程中,T 細胞會發生各種變化。當接受血管正常化等相關治療後,T 細胞更容易黏附在血管內皮細胞的表面,並滲入腫瘤組織內,從而引發更強烈的局部炎症反應。這種炎症反應又會促使腫瘤細胞或血管內皮細胞表達出更多的 PD-L1,進而抑制 T 細胞的活動。此時,雖然大部分滲入腫瘤部位的 T 細胞仍然具有活性,能夠釋放促炎因子並殺死腫瘤細胞,但這些促炎因子也會導致腫瘤細胞表達出PD-L1,從而使腫瘤細胞能夠逃避免疫細胞的攻擊。
不過,通過其他免疫編輯正常化策略,可以提升 T 細胞對腫瘤細胞的殺傷能力,當阻斷 PD-1/PD-L1 通路,這反而會有助於促進具有幹細胞特性的 T 細胞的增殖,進而提升 T 細胞的殺傷腫瘤之功能。
長期而言,持續的抗原刺激或促炎因子的影響,會導致 TCF-1 的表達下降、T 細胞的幹細胞特性喪失,以及細胞激素的釋放能力降低。在這個階段,腫瘤部位的大部分效應細胞都會進入終末耗竭的狀態,從而失去識別和殺死腫瘤細胞的能力。如果能在這個階段對腫瘤細胞進行干預,可以改變癌細胞的表觀遺傳學特性和代謝過程,從而降低癌細胞的存活能力,並減輕 T 細胞的耗竭狀態。如此一來,就能持續抑制癌細胞的增殖,甚至有可能使腫瘤消退。
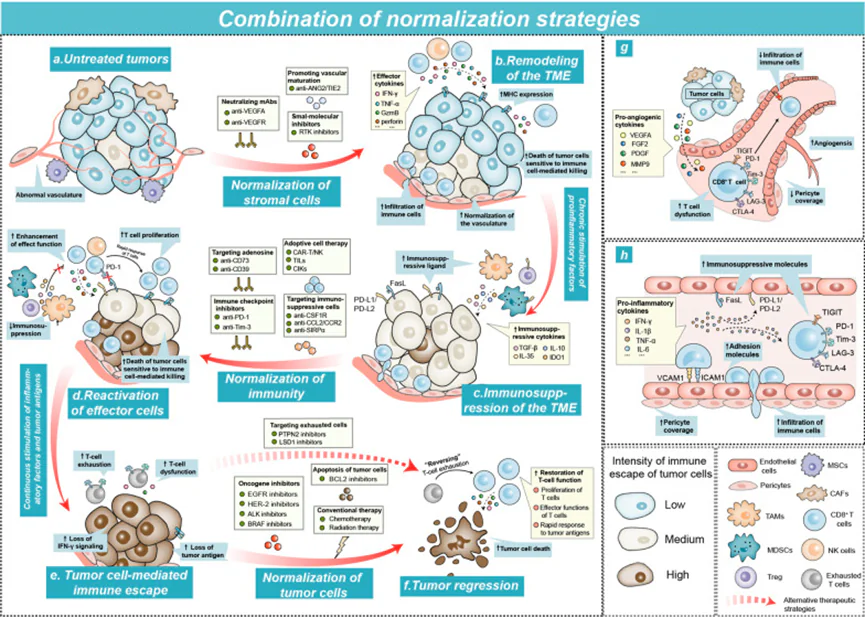
免疫編輯正常化治療後,腫瘤微環境( TME)中的微觀變化模型。
a–f 圖顯示了在正常化治療的綜合作用下,TME 所發生的一系列變化。
a 代表未經治療的腫瘤微環境;
b 代表經過間質細胞正常化治療後的 腫瘤微環境;
c 代表因持續的促炎因子刺激而呈現免疫抑制狀態的腫瘤微環境;
d 代表經過免疫系統正常化治療後的腫瘤微環境;
e 代表在持續的炎症因子作用下,由腫瘤細胞所引發的免疫逃逸所形成的腫瘤微環境;
f 代表經過腫瘤細胞正常化治療後,腫瘤出現消退的狀態;
g 描述了未經治療的腫瘤微環境中,免疫細胞在血管內的動態變化;
h 描述了經過間質細胞正常化治療後,免疫細胞在血管內的動態變化
免疫編輯之平衡階段的特性與對抗免疫編輯的策略:適應性免疫系統與先天性免疫系統的相互協同作用
當癌症免疫編輯過程處於平衡階段時,癌細胞與免疫系統之間的互動就會變得更加隱蔽。未被抑制的癌細胞與仍具有免疫功能的免疫系統之間,存在著一種動態的平衡,但這種平衡只是相對的,而非絕對的。
根據該領域的先前觀點,適應性免疫系統在維持這種平衡狀態中起著重要作用。然而,最近的研究證實,先天免疫系統也可能參與其中,在適應性免疫系統中,CD8+ T 細胞一直被視為控制腫瘤生長的重要細胞類型。研究發現,將腦膠質瘤植入缺乏 CD8+ T 細胞的小鼠體內後,更容易形成腫瘤。Park 等人也提出了類似的觀點。研究發現,那些常駐在組織中的 CD8+ T 細胞,有助於維持黑色素瘤細胞與免疫系統之間的長期平衡。此外,如果小鼠失去了CD8+ T細胞,這種平衡就會更容易被破壞,黑色素瘤細胞也會更易於生長。這些研究結果表明,在癌症免疫調節的平衡階段,適應性免疫系統和先天免疫系統在監控和抑制腫瘤生長方面,是具有協同的作用。
在平衡階段,多數腫瘤並不會表現出明顯的腫瘤特徵,甚至可能長期維持在這種動態平衡狀態中。Koebel 等人發現,用化學致癌物甲基膽蒽處理過的小鼠,其癌細胞可在體內潛伏 100 天以上,直到使用免疫抑制劑後,腫瘤組織才又被發現。除了動物實驗之外,臨床上也有類似的案例:有兩名接受腎臟移植的患者,在移植後被診斷出患有轉移性黑色素瘤。對捐贈者的醫療記錄進行檢查後發現,該捐贈者本身就有黑色素瘤的病史,且已經完全康復已經超過 10 年之久。此外,巴雷特食道轉變為食道腺癌的過程也屬於平衡階段,這個過程可能持續長達 30 年。這些現象都說明瞭免疫平衡階段的長期性、潛伏性以及難以被觀察到的特點。因此,當癌症的免疫修飾過程處於平衡階段時,臨床上的挑戰是在於如何確定患者是否處於此階段,以及應該採取何種處理措施。
由於處於平衡期的癌症缺乏明顯的特徵,因此很難在臨床上被發現。正因如此,學界也沒有對處於平衡期的腫瘤給出明確的定義。例如,體內的大部分黑色素細胞都是良性的,它們沒有增殖或分裂的能力。不過,有些良性黑色素細胞在受到紫外線或其他外部刺激後可能會變成癌細胞,從而重新獲得增殖能力。正常黑色素細胞向黑色素瘤的轉變過程,就屬於平衡期。在這個階段,惡性黑色素瘤細胞會與免疫系統積極互動;有研究指出,20%到 30%的黑色素瘤會自發性地消退,這主要是因為黑色素瘤的高度異質性與免疫反應之間存在密切關聯,這使得黑色素瘤更容易受到體內 CD4+和 CD8+T 細胞的調節。此外,研究人員還發現,腫瘤的自發消退與感染、炎症以及手術等因素是有關的。這也說明癌症免疫編輯在免疫系統與唉細胞的互動中所扮演的重要角色,同時也說明使用免疫治療的介入下,處於平衡期的癌症有可能進入免疫消除期。
另一個例子是肺部的玻璃樣結節或實質性顆粒。由於這些實質性及玻璃樣結節大多是由於發炎反應所引起的良性病變,因此常常被忽略。不過,有些發育緩慢或無法消退的玻璃樣結節,可能屬於肺原位腺癌或早期肺癌;在這些持續存在的玻璃樣結節中,有 29%到 34%被診斷為惡性。然而,雖然玻璃樣結節在組織學上屬於惡性,但其在臨床上往往表現得不活躍,且發展為肺腺癌的機率通常較低。因此,臨床實務中對此主要採取長期觀察的方式,以避免不必要的醫療處理和資源浪費。Xiao 等人通過單細胞測序發現,亞實質性結節型肺癌中 CD8+ T 細胞的浸潤程度比實質性結節型肺癌更高,而兩者中 NK 細胞的浸潤程度都較低。這一特點與適應性免疫系統的活躍作用以及先天免疫系統的功能障礙相符合。在從平衡階段轉變為免役逃逸階段的過程中,肺癌患者肺部的玻璃樣結節中,CD8 + T 細胞的數量明顯低於腫瘤組織中 CD8 + T 細胞的數量。同時,玻璃樣結節中腫瘤相關巨噬細胞(TAM)的浸潤程度則明顯增加。這些結果表明,玻璃樣結節中的免疫細胞浸潤程度較低,並暗示腫瘤細胞可能在惡性化的過程中,會誘導了 TAMs 的更多浸潤。 這個過程顯示了癌細胞從平衡狀態轉變為免役逃逸狀態的可能模式。
此外,T 細胞對癌細胞中新抗原的識別,是維持癌症免疫調節過程中平衡狀態的關鍵。腫瘤組織中的免疫反應強度,也可作為判斷腫瘤是否從平衡狀態轉入“逃逸狀態”的指標,尤其是在那些以免疫炎症為主的腫瘤微環境中。Desai 等人認為,這種平衡狀態與 TIME 有密切關係。在“熱型 TIME”中,腫瘤組織中的免疫活動更為活躍且持續,這表明免疫系統正在積極地抑制腫瘤的生長;但同時,也意味著腫瘤組織有可能轉入“免疫逃逸狀態”。基於這些研究結果,Desai 等人建議,針對處於平衡狀態的腫瘤,如果進行免疫治療,可以有效地幫助患者儘可能長時間維持這種平衡狀態。不過,目前處於平衡狀態的腫瘤大多通過手術治療。
那些依賴於手術切除可見的癌變組織以及輔助化學治療的治療方式,其在應對癌症的免疫調節機制這一複雜過程時,其實效果是十分有限。雖然這些方法能夠暫時控制腫瘤,但無法防止癌症的復發或阻擋癌症的進展,因此患者仍面臨著疾病繼續惡化的風險。為了應對這些挑戰,一種新的治療策略被引入臨床實務,即術前的輔助免疫治療:也就是先進行全身性免疫治療,再進行手術。與手術後的輔助治療相比,術前輔助免疫治療能夠讓更多的腫瘤抗原呈現給循環系統中的特定 T 細胞,從而更有效地啟動預防或抵消癌症的免疫調節機制。在治療處於穩定期狀態的癌症時,應重視全身免疫系統的狀態,並採取相對應的干預措施。
在過去十年左右的時間裡,癌症疫苗在癌症治療方面並未取得令人滿意的成果。只有 Sipuleucel-T 因其在前列腺癌治療中的出色效果而獲得了美國 FDA 的核准。由於腫瘤微環境的高度異質性以及其對免疫系統的抑制作用,疫苗的有效性受到了嚴重限制。而癌症疫苗治療成功的必要條件,包括:較低的腫瘤負荷、較弱的免疫抑制環境,以及活躍的適應性免疫反應。這些條件與腫瘤處於平衡期的特徵相符合。在該階段,腫瘤負荷也較低,適應性免疫功能也尚未受到破壞。因此,在腫瘤處於平衡期時給予癌症疫苗的治療,可能是一種有效的方法,能夠阻止癌症的惡化。
mRNA 疫苗在對抗 COVID-19 的過程中表現出色,同時也被視為癌症治療的潛在方案。與傳統疫苗相比,mRNA 疫苗能夠同時編碼多種與腫瘤相關的抗原或新抗原,從而促進適應性免疫反應。此外,mRNA 疫苗還具有生產速度快、成本低且安全性高的優點,這有助於縮短藥物研發及臨床試驗的時間。鑒於 mRNA 疫苗的這些優點,包括 CureVac、BioNTech 和 Moderna 在內的多家公司都加快了 mRNA 疫苗的研發進度,尤其是針對個體化治療的疫苗。
免疫編輯之免疫清除階段的特徵與對抗免疫編輯的策略:先天免疫系統承擔著重要的功能
當癌症的免疫調節過程處於清除階段時,先天免疫系統主要承擔著清除癌細胞的任務。Kim 等人曾在之前的研究中討論了免疫系統在消除階段清除癌細胞的機制。這個過程始於先天免疫細胞,尤其是自然殺手(NK) 細胞,對癌細胞的識別與殺死。這是一個快速且有效的過程。
此外,正常細胞轉變為癌細胞,或是癌細胞出現上皮間質轉化,都可能導致癌細胞表面缺乏自然殺手細胞的抑制信號,同時 NKG2D 受體的各種配體以及細胞黏附分子 1 的表達量會上升。這些變化會激活 NK 細胞所主導的特定免疫監視功能,從而有效抑制腫瘤的轉移以及正常細胞的惡性轉化。
同樣的,自然殺手細胞也能利用 Ly49 受體來辨別那些已經失去 MHC-I 表達的癌細胞,從而防止癌細胞逃避免疫系統的攻擊。事實上,缺乏 Ly49 受體的轉基因小鼠,其乳癌的發生速度比具有正常 Ly49 受體表達的小鼠更快。此外,這些小鼠的腫瘤中存在大量的 CD69+細胞,而 Granzyme B+的 NK 細胞數量則較少。有趣的是,那些非典型的「巡邏」單核細胞,其免疫監視能力更強。與典型的炎性單核細胞相比,它們能夠釋放更多的 CCL3/4/5 蛋白質,這些蛋白質能夠吸引自然殺手細胞,從而幫助清除轉移性的腫瘤細胞。在先前的文獻中,也有許多研究證實了先天免疫系統在腫瘤消除過程中所扮演的角色。
由於免疫清除期的特性十分隱蔽,因此很少有研究探討在這個階段對免疫系統進行干預是否真的能夠降低癌症的發生率。有人認為,利用疫苗來預防腫瘤的進展,是消除期的理想解決方案。實際上,使用疫苗來預防人類乳頭瘤病毒引起的子宮頸上皮瘤以及乙型肝炎病毒引起的肝癌,確實能有效降低癌症的發生率。不過,這種疫苗主要能夠促進體內適應性免疫系統的殺傷作用,從而只消除被病毒感染的細胞,而無法顯著增強先天的免疫能力,而後天免疫的能力在免疫清除期才是最重要的。因此,疫苗很可能不是消除期最理想的干預方式。
2020 年對 755,459 名志願者進行的研究顯示,定期進行日常運動有助於降低七種癌症的風險,包括腸癌、腎癌和乳癌。其他研究也得到了類似的結果。有一些初步研究指出,自然殺手細胞在運動與癌症預防方面扮演著重要角色。
運動有助於增加循環系統中的自然殺手細胞數量,並透過提高血液中的兒茶酚胺水平,增強先天免疫系統偵測癌細胞的能力。定期的運動還能促進自然殺手細胞的毒殺作用,其方式是增加 IL-15 的分泌,並促進 NKG2D 的表達。此外,定期運動還能夠影響血液灌注、氧氣消耗和體溫等生理變化,間接影響 自然殺手細胞的功能。因此,定期運動可能是提升免疫系統功能的重要方式,進而幫助預防癌症。除了運動之外,適當的營養攝取、心理健康和充足的睡眠也有助於調節免疫系統。
營養與飲食對免疫系統的影響已經有大量研究,其相關機制也已被充分證實。缺乏維生素及微量營養素(如鋅、銅、鐵)會削弱自然殺手細胞的活性、巨噬細胞的吞噬功能,以及 T 細胞的殺傷能力。而透過飲食補充這些營養素,可以有效地提升免疫系統的功能。
對於那些營養狀況不佳的人來說,補充營養素可能具有預防癌症的作用。相反地,對於營養狀況良好的人來說,補充營養素反而可能會增加罹患癌症的風險。過量的營養素攝取會導致營養過剩,進而使部分多餘的營養素被儲存在脂肪組織中。脂肪量對免疫系統有顯著影響,因為瘦素是可以調節 T 細胞的活化與增殖。此外,瘦素還能影響巨噬細胞的吞噬作用、細胞激素的產生,以及讓巨噬細胞朝向 M1 型巨噬細胞的轉化過程。
有人發現,白色脂肪組織中富含具有記憶功能的淋巴細胞,這些淋巴細胞有助於免疫監視和長期的防禦作用]。然而,過度的脂肪累積會導致肥胖,而肥胖又會嚴重損害免疫系統的功能。因高脂肪飲食引起的肥胖會改變腫瘤中的脂肪酸分佈,降低 CD8+ T 細胞的滲透能力和功能,並加速腫瘤的生長。
此外,肥胖還會破壞 自然殺手細胞的正常代謝和運輸功能,因為它會導致過氧化物酶體增殖激活受體(PPAR)所調控的脂質累積,進而嚴重削弱自然殺手細胞的細胞毒殺性。Hahn 等人對 800 隻老年小鼠進行了研究,發現那些長期保持低脂飲食的小鼠,其壽命比那些隨意進食的小鼠更長。這說明,為了維持最佳的免疫功能並延緩衰老,保持長期均衡的飲食和適當的營養攝取非常重要。
同樣的,心理和情緒因素對於身體的免疫功能也同樣重要。短期或急性的壓力可能會提升免疫系統的功能;Dopp 等人發現,因婚姻衝突所引起的急性壓力,會增加血液中自然殺手細胞和 CD8+T 細胞的數量,同時也提升了自然殺手細胞的細胞毒殺性。
此外,短期壓力還可以通過影響腎上腺激素及各種細胞激素的濃度(例如 IL-1a、TNF 和 IL-6),來提升巨噬細胞和 CD8+T 細胞的功能及遷移能力,同時也有助於免疫記憶的形成。
而慢性壓力、抑鬱和焦慮則會抑制免疫功能;在這些狀態下,中樞神經系統會促使體內產生大量皮質類固醇,從而抑制巨噬細胞和 T 細胞的功能。研究還發現,在配偶去世等情況所導致的情緒波動期間,皮質類固醇的水平會明顯上升,而 自然殺手細胞的活性則會明顯下降。因此,維持心理健康是維持免疫系統正常功能的重要策略。
早在 2007 年,人體的生理節律失調就被認定為一種可能的致癌因素。也就是說,生理時鐘的紊亂和睡眠障礙會大幅降低褪黑激素的水平,而褪黑激素與乳癌的發生有密切關聯。Cortés-Hernández 等人指出,生理節律與循環腫瘤細胞的免疫逃逸機制之間存在著重要的關聯:在生理節律不利的時期,循環腫瘤細胞會減少或限制其免疫的活動;而在生理節律有利的時期,它們則會增強免疫的活動性。最近,Diamantopoulou 等人證實了這樣一種觀點:循環腫瘤細胞在睡眠期間比清醒時會更容易發生轉移。這種現象與褪黑激素、睪固酮和糖皮質激素等重要的生理激素有關。這一發現並不意味著睡眠會促進腫瘤的發展,而只是說循環腫瘤細胞在生理節律的特定階段會更有可能進入血液循環中。
此外,睡眠障礙和生理節律的紊亂也可能嚴重影響免疫功能。例如,在接種流感疫苗後的 10 天內,那些有多日睡眠不足(每晚只睡 4 小時)的受試者,其體內針對流感病毒的抗體水平,不到那些能保持正常睡眠時間的受試者的一半。同樣地,在接種A型肝炎疫苗時,只要 24 小時的睡眠不足,就會導致抗體水平下降;相反地,充足的睡眠則有助於增加抗原特異性的 CD4+ T 細胞數量,並促進免疫記憶的形成。 因此,在免疫清除階段,保持充足的睡眠和正常的生理節律,依然是提升免疫系統功能的重要策略。
此外,運動、營養、心理健康和睡眠不僅與免疫系統的調節有關,彼此之間也存在著密切的關聯。定期運動和充足的睡眠有助於改善心理健康,減少壓力、焦慮和抑鬱的情緒。而充足的營養攝取則有助於維持定期運動並提升睡眠品質。
因此,在免疫清除階段,應從這各個方面入手,以培養出定期運動、心理健康、充足睡眠和合理營養攝取的生活習慣。這種干預方式將有效增強先天的和後天的免疫功能,並在消除階段阻止癌症的免疫逃逸現象。(見下圖)
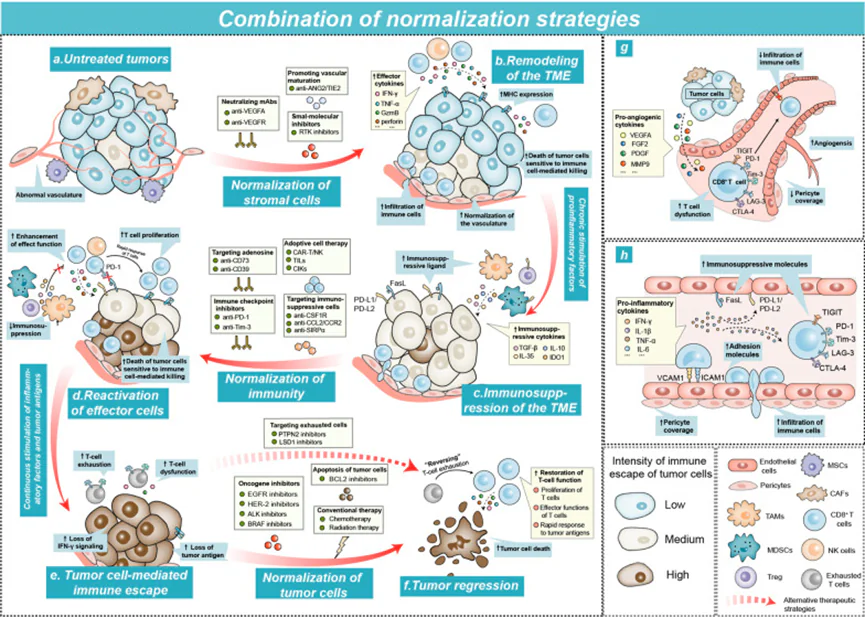
免疫編輯正常化治療後,腫瘤微環境( TME)中的微觀變化模型。
a–f 圖顯示了在正常化治療的綜合作用下,TME 所發生的一系列變化。
a 代表未經治療的腫瘤微環境;
b 代表經過間質細胞正常化治療後的 腫瘤微環境;
c 代表因持續的促炎因子刺激而呈現免疫抑制狀態的腫瘤微環境;
d 代表經過免疫系統正常化治療後的腫瘤微環境;
e 代表在持續的炎症因子作用下,由腫瘤細胞所引發的免疫逃逸所形成的腫瘤微環境;
f 代表經過腫瘤細胞正常化治療後,腫瘤出現消退的狀態;
g 描述了未經治療的腫瘤微環境中,免疫細胞在血管內的動態變化;
h 描述了經過間質細胞正常化治療後,免疫細胞在血管內的動態變化
免疫編輯之平衡階段的特性與對抗免疫編輯的策略:適應性免疫系統與先天性免疫系統的相互協同作用
當癌症免疫編輯過程處於平衡階段時,癌細胞與免疫系統之間的互動就會變得更加隱蔽。未被抑制的癌細胞與仍具有免疫功能的免疫系統之間,存在著一種動態的平衡,但這種平衡只是相對的,而非絕對的。
根據該領域的先前觀點,適應性免疫系統在維持這種平衡狀態中起著重要作用。然而,最近的研究證實,先天免疫系統也可能參與其中,在適應性免疫系統中,CD8+ T 細胞一直被視為控制腫瘤生長的重要細胞類型。研究發現,將腦膠質瘤植入缺乏 CD8+ T 細胞的小鼠體內後,更容易形成腫瘤。Park 等人也提出了類似的觀點。研究發現,那些常駐在組織中的 CD8+ T 細胞,有助於維持黑色素瘤細胞與免疫系統之間的長期平衡。此外,如果小鼠失去了CD8+ T細胞,這種平衡就會更容易被破壞,黑色素瘤細胞也會更易於生長。這些研究結果表明,在癌症免疫調節的平衡階段,適應性免疫系統和先天免疫系統在監控和抑制腫瘤生長方面,是具有協同的作用。
在平衡階段,多數腫瘤並不會表現出明顯的腫瘤特徵,甚至可能長期維持在這種動態平衡狀態中。Koebel 等人發現,用化學致癌物甲基膽蒽處理過的小鼠,其癌細胞可在體內潛伏 100 天以上,直到使用免疫抑制劑後,腫瘤組織才又被發現。除了動物實驗之外,臨床上也有類似的案例:有兩名接受腎臟移植的患者,在移植後被診斷出患有轉移性黑色素瘤。對捐贈者的醫療記錄進行檢查後發現,該捐贈者本身就有黑色素瘤的病史,且已經完全康復已經超過 10 年之久。此外,巴雷特食道轉變為食道腺癌的過程也屬於平衡階段,這個過程可能持續長達 30 年。這些現象都說明瞭免疫平衡階段的長期性、潛伏性以及難以被觀察到的特點。因此,當癌症的免疫修飾過程處於平衡階段時,臨床上的挑戰是在於如何確定患者是否處於此階段,以及應該採取何種處理措施。
由於處於平衡期的癌症缺乏明顯的特徵,因此很難在臨床上被發現。正因如此,學界也沒有對處於平衡期的腫瘤給出明確的定義。例如,體內的大部分黑色素細胞都是良性的,它們沒有增殖或分裂的能力。不過,有些良性黑色素細胞在受到紫外線或其他外部刺激後可能會變成癌細胞,從而重新獲得增殖能力。正常黑色素細胞向黑色素瘤的轉變過程,就屬於平衡期。在這個階段,惡性黑色素瘤細胞會與免疫系統積極互動;有研究指出,20%到 30%的黑色素瘤會自發性地消退,這主要是因為黑色素瘤的高度異質性與免疫反應之間存在密切關聯,這使得黑色素瘤更容易受到體內 CD4+和 CD8+T 細胞的調節。此外,研究人員還發現,腫瘤的自發消退與感染、炎症以及手術等因素是有關的。這也說明癌症免疫編輯在免疫系統與唉細胞的互動中所扮演的重要角色,同時也說明使用免疫治療的介入下,處於平衡期的癌症有可能進入免疫消除期。
另一個例子是肺部的玻璃樣結節或實質性顆粒。由於這些實質性及玻璃樣結節大多是由於發炎反應所引起的良性病變,因此常常被忽略。不過,有些發育緩慢或無法消退的玻璃樣結節,可能屬於肺原位腺癌或早期肺癌;在這些持續存在的玻璃樣結節中,有 29%到 34%被診斷為惡性。然而,雖然玻璃樣結節在組織學上屬於惡性,但其在臨床上往往表現得不活躍,且發展為肺腺癌的機率通常較低。因此,臨床實務中對此主要採取長期觀察的方式,以避免不必要的醫療處理和資源浪費。Xiao 等人通過單細胞測序發現,亞實質性結節型肺癌中 CD8+ T 細胞的浸潤程度比實質性結節型肺癌更高,而兩者中 NK 細胞的浸潤程度都較低。這一特點與適應性免疫系統的活躍作用以及先天免疫系統的功能障礙相符合。在從平衡階段轉變為免役逃逸階段的過程中,肺癌患者肺部的玻璃樣結節中,CD8 + T 細胞的數量明顯低於腫瘤組織中 CD8 + T 細胞的數量。同時,玻璃樣結節中腫瘤相關巨噬細胞(TAM)的浸潤程度則明顯增加。這些結果表明,玻璃樣結節中的免疫細胞浸潤程度較低,並暗示腫瘤細胞可能在惡性化的過程中,會誘導了 TAMs 的更多浸潤。 這個過程顯示了癌細胞從平衡狀態轉變為免役逃逸狀態的可能模式。
此外,T 細胞對癌細胞中新抗原的識別,是維持癌症免疫調節過程中平衡狀態的關鍵。腫瘤組織中的免疫反應強度,也可作為判斷腫瘤是否從平衡狀態轉入“逃逸狀態”的指標,尤其是在那些以免疫炎症為主的腫瘤微環境中。Desai 等人認為,這種平衡狀態與 TIME 有密切關係。在“熱型 TIME”中,腫瘤組織中的免疫活動更為活躍且持續,這表明免疫系統正在積極地抑制腫瘤的生長;但同時,也意味著腫瘤組織有可能轉入“免疫逃逸狀態”。基於這些研究結果,Desai 等人建議,針對處於平衡狀態的腫瘤,如果進行免疫治療,可以有效地幫助患者儘可能長時間維持這種平衡狀態。不過,目前處於平衡狀態的腫瘤大多通過手術治療。
那些依賴於手術切除可見的癌變組織以及輔助化學治療的治療方式,其在應對癌症的免疫調節機制這一複雜過程時,其實效果是十分有限。雖然這些方法能夠暫時控制腫瘤,但無法防止癌症的復發或阻擋癌症的進展,因此患者仍面臨著疾病繼續惡化的風險。為了應對這些挑戰,一種新的治療策略被引入臨床實務,即術前的輔助免疫治療:也就是先進行全身性免疫治療,再進行手術。與手術後的輔助治療相比,術前輔助免疫治療能夠讓更多的腫瘤抗原呈現給循環系統中的特定 T 細胞,從而更有效地啟動預防或抵消癌症的免疫調節機制。在治療處於穩定期狀態的癌症時,應重視全身免疫系統的狀態,並採取相對應的干預措施。
在過去十年左右的時間裡,癌症疫苗在癌症治療方面並未取得令人滿意的成果。只有 Sipuleucel-T 因其在前列腺癌治療中的出色效果而獲得了美國 FDA 的核准。由於腫瘤微環境的高度異質性以及其對免疫系統的抑制作用,疫苗的有效性受到了嚴重限制。而癌症疫苗治療成功的必要條件,包括:較低的腫瘤負荷、較弱的免疫抑制環境,以及活躍的適應性免疫反應。這些條件與腫瘤處於平衡期的特徵相符合。在該階段,腫瘤負荷也較低,適應性免疫功能也尚未受到破壞。因此,在腫瘤處於平衡期時給予癌症疫苗的治療,可能是一種有效的方法,能夠阻止癌症的惡化。
mRNA 疫苗在對抗 COVID-19 的過程中表現出色,同時也被視為癌症治療的潛在方案。與傳統疫苗相比,mRNA 疫苗能夠同時編碼多種與腫瘤相關的抗原或新抗原,從而促進適應性免疫反應。此外,mRNA 疫苗還具有生產速度快、成本低且安全性高的優點,這有助於縮短藥物研發及臨床試驗的時間。鑒於 mRNA 疫苗的這些優點,包括 CureVac、BioNTech 和 Moderna 在內的多家公司都加快了 mRNA 疫苗的研發進度,尤其是針對個體化治療的疫苗。
免疫編輯之免疫清除階段的特徵與對抗免疫編輯的策略:先天免疫系統承擔著重要的功能
當癌症的免疫調節過程處於清除階段時,先天免疫系統主要承擔著清除癌細胞的任務。Kim 等人曾在之前的研究中討論了免疫系統在消除階段清除癌細胞的機制。這個過程始於先天免疫細胞,尤其是自然殺手(NK) 細胞,對癌細胞的識別與殺死。這是一個快速且有效的過程。
此外,正常細胞轉變為癌細胞,或是癌細胞出現上皮間質轉化,都可能導致癌細胞表面缺乏自然殺手細胞的抑制信號,同時 NKG2D 受體的各種配體以及細胞黏附分子 1 的表達量會上升。這些變化會激活 NK 細胞所主導的特定免疫監視功能,從而有效抑制腫瘤的轉移以及正常細胞的惡性轉化。
同樣的,自然殺手細胞也能利用 Ly49 受體來辨別那些已經失去 MHC-I 表達的癌細胞,從而防止癌細胞逃避免疫系統的攻擊。事實上,缺乏 Ly49 受體的轉基因小鼠,其乳癌的發生速度比具有正常 Ly49 受體表達的小鼠更快。此外,這些小鼠的腫瘤中存在大量的 CD69+細胞,而 Granzyme B+的 NK 細胞數量則較少。有趣的是,那些非典型的「巡邏」單核細胞,其免疫監視能力更強。與典型的炎性單核細胞相比,它們能夠釋放更多的 CCL3/4/5 蛋白質,這些蛋白質能夠吸引自然殺手細胞,從而幫助清除轉移性的腫瘤細胞。在先前的文獻中,也有許多研究證實了先天免疫系統在腫瘤消除過程中所扮演的角色。
由於免疫清除期的特性十分隱蔽,因此很少有研究探討在這個階段對免疫系統進行干預是否真的能夠降低癌症的發生率。有人認為,利用疫苗來預防腫瘤的進展,是消除期的理想解決方案。實際上,使用疫苗來預防人類乳頭瘤病毒引起的子宮頸上皮瘤以及乙型肝炎病毒引起的肝癌,確實能有效降低癌症的發生率。不過,這種疫苗主要能夠促進體內適應性免疫系統的殺傷作用,從而只消除被病毒感染的細胞,而無法顯著增強先天的免疫能力,而後天免疫的能力在免疫清除期才是最重要的。因此,疫苗很可能不是消除期最理想的干預方式。
2020 年對 755,459 名志願者進行的研究顯示,定期進行日常運動有助於降低七種癌症的風險,包括腸癌、腎癌和乳癌。其他研究也得到了類似的結果。有一些初步研究指出,自然殺手細胞在運動與癌症預防方面扮演著重要角色。
運動有助於增加循環系統中的自然殺手細胞數量,並透過提高血液中的兒茶酚胺水平,增強先天免疫系統偵測癌細胞的能力。定期的運動還能促進自然殺手細胞的毒殺作用,其方式是增加 IL-15 的分泌,並促進 NKG2D 的表達。此外,定期運動還能夠影響血液灌注、氧氣消耗和體溫等生理變化,間接影響 自然殺手細胞的功能。因此,定期運動可能是提升免疫系統功能的重要方式,進而幫助預防癌症。除了運動之外,適當的營養攝取、心理健康和充足的睡眠也有助於調節免疫系統。
營養與飲食對免疫系統的影響已經有大量研究,其相關機制也已被充分證實。缺乏維生素及微量營養素(如鋅、銅、鐵)會削弱自然殺手細胞的活性、巨噬細胞的吞噬功能,以及 T 細胞的殺傷能力。而透過飲食補充這些營養素,可以有效地提升免疫系統的功能。
對於那些營養狀況不佳的人來說,補充營養素可能具有預防癌症的作用。相反地,對於營養狀況良好的人來說,補充營養素反而可能會增加罹患癌症的風險。過量的營養素攝取會導致營養過剩,進而使部分多餘的營養素被儲存在脂肪組織中。脂肪量對免疫系統有顯著影響,因為瘦素是可以調節 T 細胞的活化與增殖。此外,瘦素還能影響巨噬細胞的吞噬作用、細胞激素的產生,以及讓巨噬細胞朝向 M1 型巨噬細胞的轉化過程。
有人發現,白色脂肪組織中富含具有記憶功能的淋巴細胞,這些淋巴細胞有助於免疫監視和長期的防禦作用]。然而,過度的脂肪累積會導致肥胖,而肥胖又會嚴重損害免疫系統的功能。因高脂肪飲食引起的肥胖會改變腫瘤中的脂肪酸分佈,降低 CD8+ T 細胞的滲透能力和功能,並加速腫瘤的生長。
此外,肥胖還會破壞 自然殺手細胞的正常代謝和運輸功能,因為它會導致過氧化物酶體增殖激活受體(PPAR)所調控的脂質累積,進而嚴重削弱自然殺手細胞的細胞毒殺性。Hahn 等人對 800 隻老年小鼠進行了研究,發現那些長期保持低脂飲食的小鼠,其壽命比那些隨意進食的小鼠更長。這說明,為了維持最佳的免疫功能並延緩衰老,保持長期均衡的飲食和適當的營養攝取非常重要。
同樣的,心理和情緒因素對於身體的免疫功能也同樣重要。短期或急性的壓力可能會提升免疫系統的功能;Dopp 等人發現,因婚姻衝突所引起的急性壓力,會增加血液中自然殺手細胞和 CD8+T 細胞的數量,同時也提升了自然殺手細胞的細胞毒殺性。
此外,短期壓力還可以通過影響腎上腺激素及各種細胞激素的濃度(例如 IL-1a、TNF 和 IL-6),來提升巨噬細胞和 CD8+T 細胞的功能及遷移能力,同時也有助於免疫記憶的形成。
而慢性壓力、抑鬱和焦慮則會抑制免疫功能;在這些狀態下,中樞神經系統會促使體內產生大量皮質類固醇,從而抑制巨噬細胞和 T 細胞的功能。研究還發現,在配偶去世等情況所導致的情緒波動期間,皮質類固醇的水平會明顯上升,而 自然殺手細胞的活性則會明顯下降。因此,維持心理健康是維持免疫系統正常功能的重要策略。
早在 2007 年,人體的生理節律失調就被認定為一種可能的致癌因素。也就是說,生理時鐘的紊亂和睡眠障礙會大幅降低褪黑激素的水平,而褪黑激素與乳癌的發生有密切關聯。Cortés-Hernández 等人指出,生理節律與循環腫瘤細胞的免疫逃逸機制之間存在著重要的關聯:在生理節律不利的時期,循環腫瘤細胞會減少或限制其免疫的活動;而在生理節律有利的時期,它們則會增強免疫的活動性。最近,Diamantopoulou 等人證實了這樣一種觀點:循環腫瘤細胞在睡眠期間比清醒時會更容易發生轉移。這種現象與褪黑激素、睪固酮和糖皮質激素等重要的生理激素有關。這一發現並不意味著睡眠會促進腫瘤的發展,而只是說循環腫瘤細胞在生理節律的特定階段會更有可能進入血液循環中。
此外,睡眠障礙和生理節律的紊亂也可能嚴重影響免疫功能。例如,在接種流感疫苗後的 10 天內,那些有多日睡眠不足(每晚只睡 4 小時)的受試者,其體內針對流感病毒的抗體水平,不到那些能保持正常睡眠時間的受試者的一半。同樣地,在接種A型肝炎疫苗時,只要 24 小時的睡眠不足,就會導致抗體水平下降;相反地,充足的睡眠則有助於增加抗原特異性的 CD4+ T 細胞數量,並促進免疫記憶的形成。 因此,在免疫清除階段,保持充足的睡眠和正常的生理節律,依然是提升免疫系統功能的重要策略。
此外,運動、營養、心理健康和睡眠不僅與免疫系統的調節有關,彼此之間也存在著密切的關聯。定期運動和充足的睡眠有助於改善心理健康,減少壓力、焦慮和抑鬱的情緒。而充足的營養攝取則有助於維持定期運動並提升睡眠品質。
因此,在免疫清除階段,應從這各個方面入手,以培養出定期運動、心理健康、充足睡眠和合理營養攝取的生活習慣。這種干預方式將有效增強先天的和後天的免疫功能,並在消除階段阻止癌症的免疫逃逸現象。(見下圖)
免疫編輯正常化治療後,腫瘤微環境( TME)中的微觀變化模型。
a–f 圖顯示了在正常化治療的綜合作用下,TME 所發生的一系列變化。
a 代表未經治療的腫瘤微環境;
b 代表經過間質細胞正常化治療後的 腫瘤微環境;
c 代表因持續的促炎因子刺激而呈現免疫抑制狀態的腫瘤微環境;
d 代表經過免疫系統正常化治療後的腫瘤微環境;
e 代表在持續的炎症因子作用下,由腫瘤細胞所引發的免疫逃逸所形成的腫瘤微環境;
f 代表經過腫瘤細胞正常化治療後,腫瘤出現消退的狀態;
g 描述了未經治療的腫瘤微環境中,免疫細胞在血管內的動態變化;
h 描述了經過間質細胞正常化治療後,免疫細胞在血管內的動態變化
免疫編輯之平衡階段的特性與對抗免疫編輯的策略:適應性免疫系統與先天性免疫系統的相互協同作用
當癌症免疫編輯過程處於平衡階段時,癌細胞與免疫系統之間的互動就會變得更加隱蔽。未被抑制的癌細胞與仍具有免疫功能的免疫系統之間,存在著一種動態的平衡,但這種平衡只是相對的,而非絕對的。
根據該領域的先前觀點,適應性免疫系統在維持這種平衡狀態中起著重要作用。然而,最近的研究證實,先天免疫系統也可能參與其中,在適應性免疫系統中,CD8+ T 細胞一直被視為控制腫瘤生長的重要細胞類型。研究發現,將腦膠質瘤植入缺乏 CD8+ T 細胞的小鼠體內後,更容易形成腫瘤。Park 等人也提出了類似的觀點。研究發現,那些常駐在組織中的 CD8+ T 細胞,有助於維持黑色素瘤細胞與免疫系統之間的長期平衡。此外,如果小鼠失去了CD8+ T細胞,這種平衡就會更容易被破壞,黑色素瘤細胞也會更易於生長。這些研究結果表明,在癌症免疫調節的平衡階段,適應性免疫系統和先天免疫系統在監控和抑制腫瘤生長方面,是具有協同的作用。
在平衡階段,多數腫瘤並不會表現出明顯的腫瘤特徵,甚至可能長期維持在這種動態平衡狀態中。Koebel 等人發現,用化學致癌物甲基膽蒽處理過的小鼠,其癌細胞可在體內潛伏 100 天以上,直到使用免疫抑制劑後,腫瘤組織才又被發現。除了動物實驗之外,臨床上也有類似的案例:有兩名接受腎臟移植的患者,在移植後被診斷出患有轉移性黑色素瘤。對捐贈者的醫療記錄進行檢查後發現,該捐贈者本身就有黑色素瘤的病史,且已經完全康復已經超過 10 年之久。此外,巴雷特食道轉變為食道腺癌的過程也屬於平衡階段,這個過程可能持續長達 30 年。這些現象都說明瞭免疫平衡階段的長期性、潛伏性以及難以被觀察到的特點。因此,當癌症的免疫修飾過程處於平衡階段時,臨床上的挑戰是在於如何確定患者是否處於此階段,以及應該採取何種處理措施。
由於處於平衡期的癌症缺乏明顯的特徵,因此很難在臨床上被發現。正因如此,學界也沒有對處於平衡期的腫瘤給出明確的定義。例如,體內的大部分黑色素細胞都是良性的,它們沒有增殖或分裂的能力。不過,有些良性黑色素細胞在受到紫外線或其他外部刺激後可能會變成癌細胞,從而重新獲得增殖能力。正常黑色素細胞向黑色素瘤的轉變過程,就屬於平衡期。在這個階段,惡性黑色素瘤細胞會與免疫系統積極互動;有研究指出,20%到 30%的黑色素瘤會自發性地消退,這主要是因為黑色素瘤的高度異質性與免疫反應之間存在密切關聯,這使得黑色素瘤更容易受到體內 CD4+和 CD8+T 細胞的調節。此外,研究人員還發現,腫瘤的自發消退與感染、炎症以及手術等因素是有關的。這也說明癌症免疫編輯在免疫系統與唉細胞的互動中所扮演的重要角色,同時也說明使用免疫治療的介入下,處於平衡期的癌症有可能進入免疫消除期。
另一個例子是肺部的玻璃樣結節或實質性顆粒。由於這些實質性及玻璃樣結節大多是由於發炎反應所引起的良性病變,因此常常被忽略。不過,有些發育緩慢或無法消退的玻璃樣結節,可能屬於肺原位腺癌或早期肺癌;在這些持續存在的玻璃樣結節中,有 29%到 34%被診斷為惡性。然而,雖然玻璃樣結節在組織學上屬於惡性,但其在臨床上往往表現得不活躍,且發展為肺腺癌的機率通常較低。因此,臨床實務中對此主要採取長期觀察的方式,以避免不必要的醫療處理和資源浪費。Xiao 等人通過單細胞測序發現,亞實質性結節型肺癌中 CD8+ T 細胞的浸潤程度比實質性結節型肺癌更高,而兩者中 NK 細胞的浸潤程度都較低。這一特點與適應性免疫系統的活躍作用以及先天免疫系統的功能障礙相符合。在從平衡階段轉變為免役逃逸階段的過程中,肺癌患者肺部的玻璃樣結節中,CD8 + T 細胞的數量明顯低於腫瘤組織中 CD8 + T 細胞的數量。同時,玻璃樣結節中腫瘤相關巨噬細胞(TAM)的浸潤程度則明顯增加。這些結果表明,玻璃樣結節中的免疫細胞浸潤程度較低,並暗示腫瘤細胞可能在惡性化的過程中,會誘導了 TAMs 的更多浸潤。 這個過程顯示了癌細胞從平衡狀態轉變為免役逃逸狀態的可能模式。
此外,T 細胞對癌細胞中新抗原的識別,是維持癌症免疫調節過程中平衡狀態的關鍵。腫瘤組織中的免疫反應強度,也可作為判斷腫瘤是否從平衡狀態轉入“逃逸狀態”的指標,尤其是在那些以免疫炎症為主的腫瘤微環境中。Desai 等人認為,這種平衡狀態與 TIME 有密切關係。在“熱型 TIME”中,腫瘤組織中的免疫活動更為活躍且持續,這表明免疫系統正在積極地抑制腫瘤的生長;但同時,也意味著腫瘤組織有可能轉入“免疫逃逸狀態”。基於這些研究結果,Desai 等人建議,針對處於平衡狀態的腫瘤,如果進行免疫治療,可以有效地幫助患者儘可能長時間維持這種平衡狀態。不過,目前處於平衡狀態的腫瘤大多通過手術治療。
那些依賴於手術切除可見的癌變組織以及輔助化學治療的治療方式,其在應對癌症的免疫調節機制這一複雜過程時,其實效果是十分有限。雖然這些方法能夠暫時控制腫瘤,但無法防止癌症的復發或阻擋癌症的進展,因此患者仍面臨著疾病繼續惡化的風險。為了應對這些挑戰,一種新的治療策略被引入臨床實務,即術前的輔助免疫治療:也就是先進行全身性免疫治療,再進行手術。與手術後的輔助治療相比,術前輔助免疫治療能夠讓更多的腫瘤抗原呈現給循環系統中的特定 T 細胞,從而更有效地啟動預防或抵消癌症的免疫調節機制。在治療處於穩定期狀態的癌症時,應重視全身免疫系統的狀態,並採取相對應的干預措施。
在過去十年左右的時間裡,癌症疫苗在癌症治療方面並未取得令人滿意的成果。只有 Sipuleucel-T 因其在前列腺癌治療中的出色效果而獲得了美國 FDA 的核准。由於腫瘤微環境的高度異質性以及其對免疫系統的抑制作用,疫苗的有效性受到了嚴重限制。而癌症疫苗治療成功的必要條件,包括:較低的腫瘤負荷、較弱的免疫抑制環境,以及活躍的適應性免疫反應。這些條件與腫瘤處於平衡期的特徵相符合。在該階段,腫瘤負荷也較低,適應性免疫功能也尚未受到破壞。因此,在腫瘤處於平衡期時給予癌症疫苗的治療,可能是一種有效的方法,能夠阻止癌症的惡化。
mRNA 疫苗在對抗 COVID-19 的過程中表現出色,同時也被視為癌症治療的潛在方案。與傳統疫苗相比,mRNA 疫苗能夠同時編碼多種與腫瘤相關的抗原或新抗原,從而促進適應性免疫反應。此外,mRNA 疫苗還具有生產速度快、成本低且安全性高的優點,這有助於縮短藥物研發及臨床試驗的時間。鑒於 mRNA 疫苗的這些優點,包括 CureVac、BioNTech 和 Moderna 在內的多家公司都加快了 mRNA 疫苗的研發進度,尤其是針對個體化治療的疫苗。
免疫編輯之免疫清除階段的特徵與對抗免疫編輯的策略:先天免疫系統承擔著重要的功能
當癌症的免疫調節過程處於清除階段時,先天免疫系統主要承擔著清除癌細胞的任務。Kim 等人曾在之前的研究中討論了免疫系統在消除階段清除癌細胞的機制。這個過程始於先天免疫細胞,尤其是自然殺手(NK) 細胞,對癌細胞的識別與殺死。這是一個快速且有效的過程。
此外,正常細胞轉變為癌細胞,或是癌細胞出現上皮間質轉化,都可能導致癌細胞表面缺乏自然殺手細胞的抑制信號,同時 NKG2D 受體的各種配體以及細胞黏附分子 1 的表達量會上升。這些變化會激活 NK 細胞所主導的特定免疫監視功能,從而有效抑制腫瘤的轉移以及正常細胞的惡性轉化。
同樣的,自然殺手細胞也能利用 Ly49 受體來辨別那些已經失去 MHC-I 表達的癌細胞,從而防止癌細胞逃避免疫系統的攻擊。事實上,缺乏 Ly49 受體的轉基因小鼠,其乳癌的發生速度比具有正常 Ly49 受體表達的小鼠更快。此外,這些小鼠的腫瘤中存在大量的 CD69+細胞,而 Granzyme B+的 NK 細胞數量則較少。有趣的是,那些非典型的「巡邏」單核細胞,其免疫監視能力更強。與典型的炎性單核細胞相比,它們能夠釋放更多的 CCL3/4/5 蛋白質,這些蛋白質能夠吸引自然殺手細胞,從而幫助清除轉移性的腫瘤細胞。在先前的文獻中,也有許多研究證實了先天免疫系統在腫瘤消除過程中所扮演的角色。
由於免疫清除期的特性十分隱蔽,因此很少有研究探討在這個階段對免疫系統進行干預是否真的能夠降低癌症的發生率。有人認為,利用疫苗來預防腫瘤的進展,是消除期的理想解決方案。實際上,使用疫苗來預防人類乳頭瘤病毒引起的子宮頸上皮瘤以及乙型肝炎病毒引起的肝癌,確實能有效降低癌症的發生率。不過,這種疫苗主要能夠促進體內適應性免疫系統的殺傷作用,從而只消除被病毒感染的細胞,而無法顯著增強先天的免疫能力,而後天免疫的能力在免疫清除期才是最重要的。因此,疫苗很可能不是消除期最理想的干預方式。
2020 年對 755,459 名志願者進行的研究顯示,定期進行日常運動有助於降低七種癌症的風險,包括腸癌、腎癌和乳癌。其他研究也得到了類似的結果。有一些初步研究指出,自然殺手細胞在運動與癌症預防方面扮演著重要角色。
運動有助於增加循環系統中的自然殺手細胞數量,並透過提高血液中的兒茶酚胺水平,增強先天免疫系統偵測癌細胞的能力。定期的運動還能促進自然殺手細胞的毒殺作用,其方式是增加 IL-15 的分泌,並促進 NKG2D 的表達。此外,定期運動還能夠影響血液灌注、氧氣消耗和體溫等生理變化,間接影響 自然殺手細胞的功能。因此,定期運動可能是提升免疫系統功能的重要方式,進而幫助預防癌症。除了運動之外,適當的營養攝取、心理健康和充足的睡眠也有助於調節免疫系統。
營養與飲食對免疫系統的影響已經有大量研究,其相關機制也已被充分證實。缺乏維生素及微量營養素(如鋅、銅、鐵)會削弱自然殺手細胞的活性、巨噬細胞的吞噬功能,以及 T 細胞的殺傷能力。而透過飲食補充這些營養素,可以有效地提升免疫系統的功能。
對於那些營養狀況不佳的人來說,補充營養素可能具有預防癌症的作用。相反地,對於營養狀況良好的人來說,補充營養素反而可能會增加罹患癌症的風險。過量的營養素攝取會導致營養過剩,進而使部分多餘的營養素被儲存在脂肪組織中。脂肪量對免疫系統有顯著影響,因為瘦素是可以調節 T 細胞的活化與增殖。此外,瘦素還能影響巨噬細胞的吞噬作用、細胞激素的產生,以及讓巨噬細胞朝向 M1 型巨噬細胞的轉化過程。
有人發現,白色脂肪組織中富含具有記憶功能的淋巴細胞,這些淋巴細胞有助於免疫監視和長期的防禦作用]。然而,過度的脂肪累積會導致肥胖,而肥胖又會嚴重損害免疫系統的功能。因高脂肪飲食引起的肥胖會改變腫瘤中的脂肪酸分佈,降低 CD8+ T 細胞的滲透能力和功能,並加速腫瘤的生長。
此外,肥胖還會破壞 自然殺手細胞的正常代謝和運輸功能,因為它會導致過氧化物酶體增殖激活受體(PPAR)所調控的脂質累積,進而嚴重削弱自然殺手細胞的細胞毒殺性。Hahn 等人對 800 隻老年小鼠進行了研究,發現那些長期保持低脂飲食的小鼠,其壽命比那些隨意進食的小鼠更長。這說明,為了維持最佳的免疫功能並延緩衰老,保持長期均衡的飲食和適當的營養攝取非常重要。
同樣的,心理和情緒因素對於身體的免疫功能也同樣重要。短期或急性的壓力可能會提升免疫系統的功能;Dopp 等人發現,因婚姻衝突所引起的急性壓力,會增加血液中自然殺手細胞和 CD8+T 細胞的數量,同時也提升了自然殺手細胞的細胞毒殺性。
此外,短期壓力還可以通過影響腎上腺激素及各種細胞激素的濃度(例如 IL-1a、TNF 和 IL-6),來提升巨噬細胞和 CD8+T 細胞的功能及遷移能力,同時也有助於免疫記憶的形成。
而慢性壓力、抑鬱和焦慮則會抑制免疫功能;在這些狀態下,中樞神經系統會促使體內產生大量皮質類固醇,從而抑制巨噬細胞和 T 細胞的功能。研究還發現,在配偶去世等情況所導致的情緒波動期間,皮質類固醇的水平會明顯上升,而 自然殺手細胞的活性則會明顯下降。因此,維持心理健康是維持免疫系統正常功能的重要策略。
早在 2007 年,人體的生理節律失調就被認定為一種可能的致癌因素。也就是說,生理時鐘的紊亂和睡眠障礙會大幅降低褪黑激素的水平,而褪黑激素與乳癌的發生有密切關聯。Cortés-Hernández 等人指出,生理節律與循環腫瘤細胞的免疫逃逸機制之間存在著重要的關聯:在生理節律不利的時期,循環腫瘤細胞會減少或限制其免疫的活動;而在生理節律有利的時期,它們則會增強免疫的活動性。最近,Diamantopoulou 等人證實了這樣一種觀點:循環腫瘤細胞在睡眠期間比清醒時會更容易發生轉移。這種現象與褪黑激素、睪固酮和糖皮質激素等重要的生理激素有關。這一發現並不意味著睡眠會促進腫瘤的發展,而只是說循環腫瘤細胞在生理節律的特定階段會更有可能進入血液循環中。
此外,睡眠障礙和生理節律的紊亂也可能嚴重影響免疫功能。例如,在接種流感疫苗後的 10 天內,那些有多日睡眠不足(每晚只睡 4 小時)的受試者,其體內針對流感病毒的抗體水平,不到那些能保持正常睡眠時間的受試者的一半。同樣地,在接種A型肝炎疫苗時,只要 24 小時的睡眠不足,就會導致抗體水平下降;相反地,充足的睡眠則有助於增加抗原特異性的 CD4+ T 細胞數量,並促進免疫記憶的形成。 因此,在免疫清除階段,保持充足的睡眠和正常的生理節律,依然是提升免疫系統功能的重要策略。
此外,運動、營養、心理健康和睡眠不僅與免疫系統的調節有關,彼此之間也存在著密切的關聯。定期運動和充足的睡眠有助於改善心理健康,減少壓力、焦慮和抑鬱的情緒。而充足的營養攝取則有助於維持定期運動並提升睡眠品質。
因此,在免疫清除階段,應從這各個方面入手,以培養出定期運動、心理健康、充足睡眠和合理營養攝取的生活習慣。這種干預方式將有效增強先天的和後天的免疫功能,並在消除階段阻止癌症的免疫逃逸現象。(見下圖)
免疫編輯正常化治療後,腫瘤微環境( TME)中的微觀變化模型。
a–f 圖顯示了在正常化治療的綜合作用下,TME 所發生的一系列變化。
a 代表未經治療的腫瘤微環境;
b 代表經過間質細胞正常化治療後的 腫瘤微環境;
c 代表因持續的促炎因子刺激而呈現免疫抑制狀態的腫瘤微環境;
d 代表經過免疫系統正常化治療後的腫瘤微環境;
e 代表在持續的炎症因子作用下,由腫瘤細胞所引發的免疫逃逸所形成的腫瘤微環境;
f 代表經過腫瘤細胞正常化治療後,腫瘤出現消退的狀態;
g 描述了未經治療的腫瘤微環境中,免疫細胞在血管內的動態變化;
h 描述了經過間質細胞正常化治療後,免疫細胞在血管內的動態變化
免疫編輯之平衡階段的特性與對抗免疫編輯的策略:適應性免疫系統與先天性免疫系統的相互協同作用
當癌症免疫編輯過程處於平衡階段時,癌細胞與免疫系統之間的互動就會變得更加隱蔽。未被抑制的癌細胞與仍具有免疫功能的免疫系統之間,存在著一種動態的平衡,但這種平衡只是相對的,而非絕對的。
根據該領域的先前觀點,適應性免疫系統在維持這種平衡狀態中起著重要作用。然而,最近的研究證實,先天免疫系統也可能參與其中,在適應性免疫系統中,CD8+ T 細胞一直被視為控制腫瘤生長的重要細胞類型。研究發現,將腦膠質瘤植入缺乏 CD8+ T 細胞的小鼠體內後,更容易形成腫瘤。Park 等人也提出了類似的觀點。研究發現,那些常駐在組織中的 CD8+ T 細胞,有助於維持黑色素瘤細胞與免疫系統之間的長期平衡。此外,如果小鼠失去了CD8+ T細胞,這種平衡就會更容易被破壞,黑色素瘤細胞也會更易於生長。這些研究結果表明,在癌症免疫調節的平衡階段,適應性免疫系統和先天免疫系統在監控和抑制腫瘤生長方面,是具有協同的作用。
在平衡階段,多數腫瘤並不會表現出明顯的腫瘤特徵,甚至可能長期維持在這種動態平衡狀態中。Koebel 等人發現,用化學致癌物甲基膽蒽處理過的小鼠,其癌細胞可在體內潛伏 100 天以上,直到使用免疫抑制劑後,腫瘤組織才又被發現。除了動物實驗之外,臨床上也有類似的案例:有兩名接受腎臟移植的患者,在移植後被診斷出患有轉移性黑色素瘤。對捐贈者的醫療記錄進行檢查後發現,該捐贈者本身就有黑色素瘤的病史,且已經完全康復已經超過 10 年之久。此外,巴雷特食道轉變為食道腺癌的過程也屬於平衡階段,這個過程可能持續長達 30 年。這些現象都說明瞭免疫平衡階段的長期性、潛伏性以及難以被觀察到的特點。因此,當癌症的免疫修飾過程處於平衡階段時,臨床上的挑戰是在於如何確定患者是否處於此階段,以及應該採取何種處理措施。
由於處於平衡期的癌症缺乏明顯的特徵,因此很難在臨床上被發現。正因如此,學界也沒有對處於平衡期的腫瘤給出明確的定義。例如,體內的大部分黑色素細胞都是良性的,它們沒有增殖或分裂的能力。不過,有些良性黑色素細胞在受到紫外線或其他外部刺激後可能會變成癌細胞,從而重新獲得增殖能力。正常黑色素細胞向黑色素瘤的轉變過程,就屬於平衡期。在這個階段,惡性黑色素瘤細胞會與免疫系統積極互動;有研究指出,20%到 30%的黑色素瘤會自發性地消退,這主要是因為黑色素瘤的高度異質性與免疫反應之間存在密切關聯,這使得黑色素瘤更容易受到體內 CD4+和 CD8+T 細胞的調節。此外,研究人員還發現,腫瘤的自發消退與感染、炎症以及手術等因素是有關的。這也說明癌症免疫編輯在免疫系統與唉細胞的互動中所扮演的重要角色,同時也說明使用免疫治療的介入下,處於平衡期的癌症有可能進入免疫消除期。
另一個例子是肺部的玻璃樣結節或實質性顆粒。由於這些實質性及玻璃樣結節大多是由於發炎反應所引起的良性病變,因此常常被忽略。不過,有些發育緩慢或無法消退的玻璃樣結節,可能屬於肺原位腺癌或早期肺癌;在這些持續存在的玻璃樣結節中,有 29%到 34%被診斷為惡性。然而,雖然玻璃樣結節在組織學上屬於惡性,但其在臨床上往往表現得不活躍,且發展為肺腺癌的機率通常較低。因此,臨床實務中對此主要採取長期觀察的方式,以避免不必要的醫療處理和資源浪費。Xiao 等人通過單細胞測序發現,亞實質性結節型肺癌中 CD8+ T 細胞的浸潤程度比實質性結節型肺癌更高,而兩者中 NK 細胞的浸潤程度都較低。這一特點與適應性免疫系統的活躍作用以及先天免疫系統的功能障礙相符合。在從平衡階段轉變為免役逃逸階段的過程中,肺癌患者肺部的玻璃樣結節中,CD8 + T 細胞的數量明顯低於腫瘤組織中 CD8 + T 細胞的數量。同時,玻璃樣結節中腫瘤相關巨噬細胞(TAM)的浸潤程度則明顯增加。這些結果表明,玻璃樣結節中的免疫細胞浸潤程度較低,並暗示腫瘤細胞可能在惡性化的過程中,會誘導了 TAMs 的更多浸潤。 這個過程顯示了癌細胞從平衡狀態轉變為免役逃逸狀態的可能模式。
此外,T 細胞對癌細胞中新抗原的識別,是維持癌症免疫調節過程中平衡狀態的關鍵。腫瘤組織中的免疫反應強度,也可作為判斷腫瘤是否從平衡狀態轉入“逃逸狀態”的指標,尤其是在那些以免疫炎症為主的腫瘤微環境中。Desai 等人認為,這種平衡狀態與 TIME 有密切關係。在“熱型 TIME”中,腫瘤組織中的免疫活動更為活躍且持續,這表明免疫系統正在積極地抑制腫瘤的生長;但同時,也意味著腫瘤組織有可能轉入“免疫逃逸狀態”。基於這些研究結果,Desai 等人建議,針對處於平衡狀態的腫瘤,如果進行免疫治療,可以有效地幫助患者儘可能長時間維持這種平衡狀態。不過,目前處於平衡狀態的腫瘤大多通過手術治療。
那些依賴於手術切除可見的癌變組織以及輔助化學治療的治療方式,其在應對癌症的免疫調節機制這一複雜過程時,其實效果是十分有限。雖然這些方法能夠暫時控制腫瘤,但無法防止癌症的復發或阻擋癌症的進展,因此患者仍面臨著疾病繼續惡化的風險。為了應對這些挑戰,一種新的治療策略被引入臨床實務,即術前的輔助免疫治療:也就是先進行全身性免疫治療,再進行手術。與手術後的輔助治療相比,術前輔助免疫治療能夠讓更多的腫瘤抗原呈現給循環系統中的特定 T 細胞,從而更有效地啟動預防或抵消癌症的免疫調節機制。在治療處於穩定期狀態的癌症時,應重視全身免疫系統的狀態,並採取相對應的干預措施。
在過去十年左右的時間裡,癌症疫苗在癌症治療方面並未取得令人滿意的成果。只有 Sipuleucel-T 因其在前列腺癌治療中的出色效果而獲得了美國 FDA 的核准。由於腫瘤微環境的高度異質性以及其對免疫系統的抑制作用,疫苗的有效性受到了嚴重限制。而癌症疫苗治療成功的必要條件,包括:較低的腫瘤負荷、較弱的免疫抑制環境,以及活躍的適應性免疫反應。這些條件與腫瘤處於平衡期的特徵相符合。在該階段,腫瘤負荷也較低,適應性免疫功能也尚未受到破壞。因此,在腫瘤處於平衡期時給予癌症疫苗的治療,可能是一種有效的方法,能夠阻止癌症的惡化。
mRNA 疫苗在對抗 COVID-19 的過程中表現出色,同時也被視為癌症治療的潛在方案。與傳統疫苗相比,mRNA 疫苗能夠同時編碼多種與腫瘤相關的抗原或新抗原,從而促進適應性免疫反應。此外,mRNA 疫苗還具有生產速度快、成本低且安全性高的優點,這有助於縮短藥物研發及臨床試驗的時間。鑒於 mRNA 疫苗的這些優點,包括 CureVac、BioNTech 和 Moderna 在內的多家公司都加快了 mRNA 疫苗的研發進度,尤其是針對個體化治療的疫苗。
免疫編輯之免疫清除階段的特徵與對抗免疫編輯的策略:先天免疫系統承擔著重要的功能
當癌症的免疫調節過程處於清除階段時,先天免疫系統主要承擔著清除癌細胞的任務。Kim 等人曾在之前的研究中討論了免疫系統在消除階段清除癌細胞的機制。這個過程始於先天免疫細胞,尤其是自然殺手(NK) 細胞,對癌細胞的識別與殺死。這是一個快速且有效的過程。
此外,正常細胞轉變為癌細胞,或是癌細胞出現上皮間質轉化,都可能導致癌細胞表面缺乏自然殺手細胞的抑制信號,同時 NKG2D 受體的各種配體以及細胞黏附分子 1 的表達量會上升。這些變化會激活 NK 細胞所主導的特定免疫監視功能,從而有效抑制腫瘤的轉移以及正常細胞的惡性轉化。
同樣的,自然殺手細胞也能利用 Ly49 受體來辨別那些已經失去 MHC-I 表達的癌細胞,從而防止癌細胞逃避免疫系統的攻擊。事實上,缺乏 Ly49 受體的轉基因小鼠,其乳癌的發生速度比具有正常 Ly49 受體表達的小鼠更快。此外,這些小鼠的腫瘤中存在大量的 CD69+細胞,而 Granzyme B+的 NK 細胞數量則較少。有趣的是,那些非典型的「巡邏」單核細胞,其免疫監視能力更強。與典型的炎性單核細胞相比,它們能夠釋放更多的 CCL3/4/5 蛋白質,這些蛋白質能夠吸引自然殺手細胞,從而幫助清除轉移性的腫瘤細胞。在先前的文獻中,也有許多研究證實了先天免疫系統在腫瘤消除過程中所扮演的角色。
由於免疫清除期的特性十分隱蔽,因此很少有研究探討在這個階段對免疫系統進行干預是否真的能夠降低癌症的發生率。有人認為,利用疫苗來預防腫瘤的進展,是消除期的理想解決方案。實際上,使用疫苗來預防人類乳頭瘤病毒引起的子宮頸上皮瘤以及乙型肝炎病毒引起的肝癌,確實能有效降低癌症的發生率。不過,這種疫苗主要能夠促進體內適應性免疫系統的殺傷作用,從而只消除被病毒感染的細胞,而無法顯著增強先天的免疫能力,而後天免疫的能力在免疫清除期才是最重要的。因此,疫苗很可能不是消除期最理想的干預方式。
2020 年對 755,459 名志願者進行的研究顯示,定期進行日常運動有助於降低七種癌症的風險,包括腸癌、腎癌和乳癌。其他研究也得到了類似的結果。有一些初步研究指出,自然殺手細胞在運動與癌症預防方面扮演著重要角色。
運動有助於增加循環系統中的自然殺手細胞數量,並透過提高血液中的兒茶酚胺水平,增強先天免疫系統偵測癌細胞的能力。定期的運動還能促進自然殺手細胞的毒殺作用,其方式是增加 IL-15 的分泌,並促進 NKG2D 的表達。此外,定期運動還能夠影響血液灌注、氧氣消耗和體溫等生理變化,間接影響 自然殺手細胞的功能。因此,定期運動可能是提升免疫系統功能的重要方式,進而幫助預防癌症。除了運動之外,適當的營養攝取、心理健康和充足的睡眠也有助於調節免疫系統。
營養與飲食對免疫系統的影響已經有大量研究,其相關機制也已被充分證實。缺乏維生素及微量營養素(如鋅、銅、鐵)會削弱自然殺手細胞的活性、巨噬細胞的吞噬功能,以及 T 細胞的殺傷能力。而透過飲食補充這些營養素,可以有效地提升免疫系統的功能。
對於那些營養狀況不佳的人來說,補充營養素可能具有預防癌症的作用。相反地,對於營養狀況良好的人來說,補充營養素反而可能會增加罹患癌症的風險。過量的營養素攝取會導致營養過剩,進而使部分多餘的營養素被儲存在脂肪組織中。脂肪量對免疫系統有顯著影響,因為瘦素是可以調節 T 細胞的活化與增殖。此外,瘦素還能影響巨噬細胞的吞噬作用、細胞激素的產生,以及讓巨噬細胞朝向 M1 型巨噬細胞的轉化過程。
有人發現,白色脂肪組織中富含具有記憶功能的淋巴細胞,這些淋巴細胞有助於免疫監視和長期的防禦作用]。然而,過度的脂肪累積會導致肥胖,而肥胖又會嚴重損害免疫系統的功能。因高脂肪飲食引起的肥胖會改變腫瘤中的脂肪酸分佈,降低 CD8+ T 細胞的滲透能力和功能,並加速腫瘤的生長。
此外,肥胖還會破壞 自然殺手細胞的正常代謝和運輸功能,因為它會導致過氧化物酶體增殖激活受體(PPAR)所調控的脂質累積,進而嚴重削弱自然殺手細胞的細胞毒殺性。Hahn 等人對 800 隻老年小鼠進行了研究,發現那些長期保持低脂飲食的小鼠,其壽命比那些隨意進食的小鼠更長。這說明,為了維持最佳的免疫功能並延緩衰老,保持長期均衡的飲食和適當的營養攝取非常重要。
同樣的,心理和情緒因素對於身體的免疫功能也同樣重要。短期或急性的壓力可能會提升免疫系統的功能;Dopp 等人發現,因婚姻衝突所引起的急性壓力,會增加血液中自然殺手細胞和 CD8+T 細胞的數量,同時也提升了自然殺手細胞的細胞毒殺性。
此外,短期壓力還可以通過影響腎上腺激素及各種細胞激素的濃度(例如 IL-1a、TNF 和 IL-6),來提升巨噬細胞和 CD8+T 細胞的功能及遷移能力,同時也有助於免疫記憶的形成。
而慢性壓力、抑鬱和焦慮則會抑制免疫功能;在這些狀態下,中樞神經系統會促使體內產生大量皮質類固醇,從而抑制巨噬細胞和 T 細胞的功能。研究還發現,在配偶去世等情況所導致的情緒波動期間,皮質類固醇的水平會明顯上升,而 自然殺手細胞的活性則會明顯下降。因此,維持心理健康是維持免疫系統正常功能的重要策略。
早在 2007 年,人體的生理節律失調就被認定為一種可能的致癌因素。也就是說,生理時鐘的紊亂和睡眠障礙會大幅降低褪黑激素的水平,而褪黑激素與乳癌的發生有密切關聯。Cortés-Hernández 等人指出,生理節律與循環腫瘤細胞的免疫逃逸機制之間存在著重要的關聯:在生理節律不利的時期,循環腫瘤細胞會減少或限制其免疫的活動;而在生理節律有利的時期,它們則會增強免疫的活動性。最近,Diamantopoulou 等人證實了這樣一種觀點:循環腫瘤細胞在睡眠期間比清醒時會更容易發生轉移。這種現象與褪黑激素、睪固酮和糖皮質激素等重要的生理激素有關。這一發現並不意味著睡眠會促進腫瘤的發展,而只是說循環腫瘤細胞在生理節律的特定階段會更有可能進入血液循環中。
此外,睡眠障礙和生理節律的紊亂也可能嚴重影響免疫功能。例如,在接種流感疫苗後的 10 天內,那些有多日睡眠不足(每晚只睡 4 小時)的受試者,其體內針對流感病毒的抗體水平,不到那些能保持正常睡眠時間的受試者的一半。同樣地,在接種A型肝炎疫苗時,只要 24 小時的睡眠不足,就會導致抗體水平下降;相反地,充足的睡眠則有助於增加抗原特異性的 CD4+ T 細胞數量,並促進免疫記憶的形成。 因此,在免疫清除階段,保持充足的睡眠和正常的生理節律,依然是提升免疫系統功能的重要策略。
此外,運動、營養、心理健康和睡眠不僅與免疫系統的調節有關,彼此之間也存在著密切的關聯。定期運動和充足的睡眠有助於改善心理健康,減少壓力、焦慮和抑鬱的情緒。而充足的營養攝取則有助於維持定期運動並提升睡眠品質。
因此,在免疫清除階段,應從這各個方面入手,以培養出定期運動、心理健康、充足睡眠和合理營養攝取的生活習慣。這種干預方式將有效增強先天的和後天的免疫功能,並在消除階段阻止癌症的免疫逃逸現象。(見下圖)
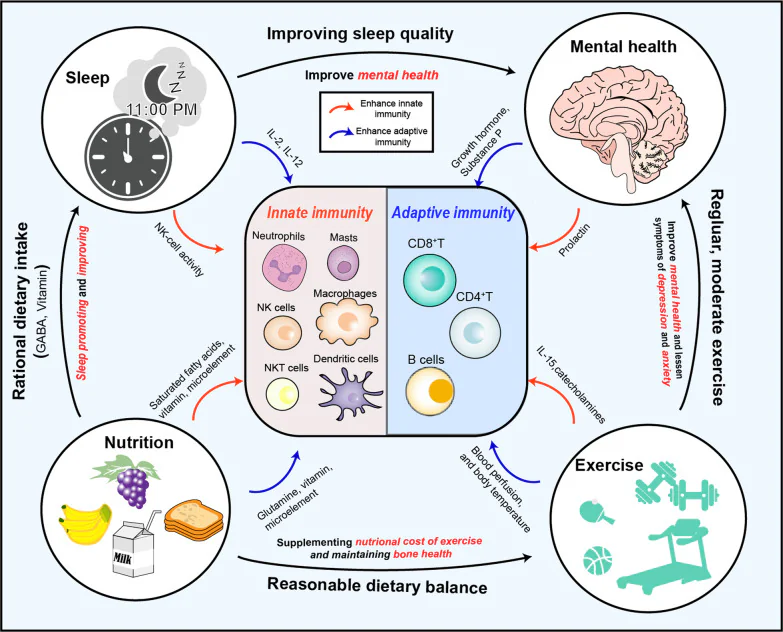
在免疫清除期中,健康的生活習慣對免疫系統有正面影響。心理健康、運動、營養和睡眠都能在清除期中協同作用,提升免疫系統的功能。
癌症免疫編輯理論解釋了癌細胞與免疫系統之間的這種矛盾關係。基於這種矛盾的關係,發展出了一套個性化且精確的免疫治療方法和方案。也就是說,透過辨別癌症免疫編輯的各個階段,並為每個階段選擇最適合的治療策略,從而促進癌症免疫編輯的逆轉,最終實現腫瘤的完全消退(見下圖)。此外,針對不同的免疫類型提出了三種治療策略。這三種治療策略可以單獨使用,也可以按特定順序搭配使用,以最大限度地提升癌症患者的生存率。
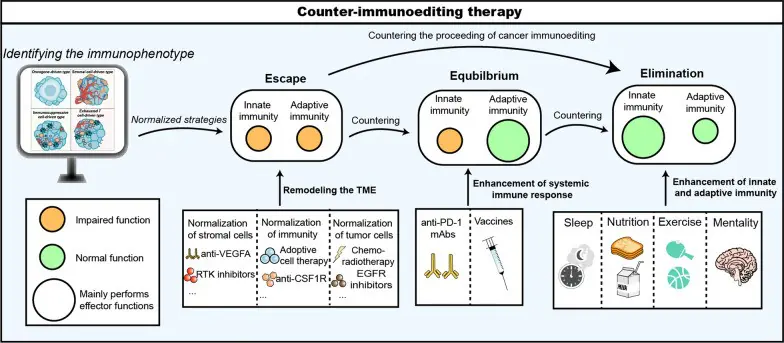
圖示:反免疫編輯治療的過程如下:
首先,患者會在初次診斷時被分類,以瞭解其免疫狀態。接下來,根據不同的免疫表型,選擇適當的治療方案。當免疫系統的狀態恢復到平衡或消除階段時,就會再選擇相應的治療方案,以幫助免疫系統有效殺死腫瘤細胞。這種方法能夠因應每個患者的獨特免疫表型,選擇最適合的治療方案,從而讓患者達到完全緩解或維持長期康復的狀態。
總之,免疫編輯正常化的策略能夠在臨床環境中,根據患者的整體免疫微環境狀況,有針對性地為患者提供合適的治療策略。同時,也在下表 中總結了免疫編輯正常化所涉及的主要治療策略與方法。
免疫逃脫階段
治療策略 | 方法 | 目標/干預措施 | 總體效果 | 對先天免疫的影響 | 對獲得性免疫的影響 |
間質細胞的標準化處理策略 | 標靶血管內皮細胞和新生血管生成(適用於基質細胞驅動型和癌基因驅動型) | 標靶:VEGF/VEGFR、PDGF/PDGFR、EGF/EGFR 等 針對血管內皮細胞及新生血管的形成進行治療 | 促進血管的正常化,並有利於效應細胞的滲透 | 增強CD8+ T細胞的功能;促進CTL和CD4+ T細胞的浸潤;減少Treg細胞的浸潤 | 促進NK細胞浸潤;防止NK細胞功能障礙;減少TAM的募集;促進DC的功能成熟;減少腫瘤相關肥大細胞的數量 |
| 標靶癌相關成纖維細胞(CAFs)(適用於基質細胞驅動型和癌基因驅動型) | 標靶:Wnt2、FAP、間皮素、TGF-β、HIF2、NetG1 等 | 增強效應細胞功能並重塑腫瘤微環境 | 恢復抗腫瘤T細胞反應;增強CD8+效應T細胞的功能;減少腫瘤浸潤性Treg細胞的數量;抑制Treg細胞的形成 | 促進NK細胞的浸潤和活化;減少M2巨噬細胞的募集;增加活性樹突狀細胞的數量;抑制肥大細胞的浸潤 |
| 標靶週細胞(適用於基質細胞驅動型和癌基因驅動型) | 標靶:DLK1、IL-33、IL-10、TGFβ、PD-L1 等 | 增強效應細胞功能並重塑腫瘤微環境 | 增強抗腫瘤T細胞反應;促進CD8+ T細胞的活化和募集;減少Treg細胞的浸潤 | 減少TAM的招聘 |
| 標靶間質幹細胞(適用於基質細胞驅動型和癌基因驅動型) | 標靶:IDO、IL-6、IL-8、IL-10、galectin-1、PGE2、activin-A 等 | 增強效應細胞功能並重塑腫瘤微環境 | 促進T細胞增殖和浸潤;促進CTL對腫瘤細胞的識別;促進B細胞浸潤和分化。 | 增強NK細胞介導的細胞毒性;抑制M2巨噬細胞極化;恢復樹突狀細胞的分化和功能;促進肥大細胞的浸潤和活化 |
免疫正常化策略 | 標靶抑制性免疫受體(適用於免疫抑制細胞驅動型和基質細胞驅動型) | 標靶:PD-1、TIGIT、VISTA、LAG3、Tim-3、CTLA-4 等 | 解除對效應細胞的免疫抑制,恢復免疫細胞的功能 | 促進效應T細胞浸潤;維持並增強效應T細胞的功能;抑制Treg細胞浸潤;增強B細胞的功能 | 防止NK細胞耗竭;增強NK細胞介導的細胞毒性 |
| 標靶免疫抑制細胞(適用於免疫抑制細胞驅動型和基質細胞驅動型) | 標靶細胞:TAM、Treg、TAN、肥大細胞、Breg 等 | 緩解免疫抑制細胞介導的免疫抑制;恢復並增強效應細胞的免疫功能 | 促進效應T細胞的活化、增殖、浸潤和功能;抑制Treg細胞的功能和增殖;抑制Breg細胞的功能。 | 促進NK細胞的活化、浸潤、增生和功能;恢復巨噬細胞的吞噬功能;抑制M2型巨噬細胞的浸潤;促進M2型巨噬細胞向M1型巨噬細胞的轉化;促進樹突狀細胞(DC)的活化;抑制腫瘤相關肥大細胞的浸潤。 |
| 標靶耗竭免疫細胞 (適用於耗竭T細胞型和基質細胞型) | 標靶:PTPN2、LSD1、CISH、TIGIT、腫瘤相關氨、腸道菌叢等 | 逆轉T細胞耗竭的功能 | 促進T細胞增殖和活化;逆轉T細胞耗竭;增強Tim-3+CD8+耗竭T細胞的效應功能和增殖能力;維持效應T細胞的幹性 | 促進NK細胞的活化、浸潤和功能;防止NK細胞耗竭 |
腫瘤細胞正常化策略 | 誘導腫瘤細胞表面抗原表達 (適用於癌基因驅動型腫瘤) | 介入:化療、放療、DNMTi、EZH2i、HDACi、IAPi 等 | 增強效應細胞對腫瘤細胞的識別 | 促進T細胞辨識和殺傷腫瘤細胞;增強T細胞功能;促進效應T細胞浸潤;減少Treg細胞的數量和功能。 | 恢復NK細胞的功能;促進DC的活化、功能和成熟 |
| 標靶抑制性配體 (適用於癌基因驅動型和免疫抑制細胞驅動型) | 標靶:PD-L1、PD-L2、半乳糖凝集素-3、LSECtin、FGL1、CD155、CD112、CEACAM-1、半乳糖凝集素-9、HMGB1、PtdSer、FasL、CD73、CD39 等 | 緩解腫瘤細胞介導的免疫抑制,增強效應細胞功能 | 促進效應T細胞的活化、增生、浸潤及功能;抑制T細胞凋亡;抑制Treg細胞活化;促進B細胞活化 | 促進NK細胞的細胞毒殺性和成熟;增強巨噬細胞的吞噬作用;促進M2型巨噬細胞向M1型巨噬細胞的轉化;促進樹突狀細胞(DC)的活化;抑制腫瘤相關肥大細胞的活化。 |
| 降低腫瘤細胞的存活率 (適用於癌基因驅動型及耗竭型T細胞驅動型腫瘤) | 介入措施:標靶代謝與表觀遺傳重編程、標靶癌基因、標靶細胞週期相關基因、標靶凋亡相關蛋白等。 | 降低腫瘤細胞的免疫逃脫能力,恢復正常的免疫功能 | 抑制T細胞凋亡並增強效應T細胞功能;促進腫瘤特異性T細胞的浸潤和再活化;減少CD4+效應調節性T細胞的浸潤;促進B細胞的浸潤 | 支持NK細胞介導的細胞毒殺性;促進NK細胞浸潤;抑制TAM活化;抑制肥大細胞活化 |
免疫平衡階段
治療策略 | 方法 | 目標/干預措施 | 總體效果 | 對先天免疫的影響 | 對獲得性免疫的影響 |
| 術前輔助治療 | 標靶:PD-1 | 促進腫瘤內和全身適應性免疫反應 | 增加T細胞克隆數量;誘導T細胞活化 | 誘導cDC1活化 |
| 癌症疫苗
| 標靶:新抗原、腫瘤相關抗原 (TAA)、腫瘤特異性抗原 (TSA) 等 介入措施:TLR 和 STING 激動劑、CD40 激動劑、溶瘤病毒等
| 促進全身適應性的免疫反應 | 誘導強烈的CD4+和CD8+ T細胞免疫反應;促進抗原特異性T細胞反應;促進T細胞浸潤;減少腫瘤內Treg細胞的數量。 | 增強NK細胞的細胞毒殺功能;促進NK細胞從M2型轉化為M1型;促進DC細胞的活化與成熟。 |
免疫清除階段
治療策略 | 方法 | 目標/干預措施 | 總體效果 | 對先天免疫的影響 | 對獲得性免疫的影響 |
| 規律運動 | 介入措施:耐力運動、有氧運動、體能訓練等 | 增強血液中自然殺手細胞(NK細胞)的功能和動員能力,維持其執行免疫監視的能力 | 促進腫瘤浸潤性IL15Rα+ CD8+ T細胞的動員和聚集;增強CD8+ T細胞的功能;增加調節性T細胞(Treg)的絕對數量;增加Treg的募集;促進未成熟B細胞的動員 | 促進NK細胞浸潤和活化;減少TAM數量;調節TAM極化;優先動員DC;促進肥大細胞浸潤和活化 |
| 合理的營養攝入 | 介入措施:補充微量營養素 | 增強適應性和先天性免疫系統反應 | 促進T細胞的成熟和增殖;保護T細胞免於凋亡;促進B細胞的增殖和效應功能。 | 增強NK細胞的細胞毒活性並維持其功能;促進巨噬細胞的發炎反應;促進樹突狀細胞(DC)的成熟和分化;恢復腫瘤相關DC的功能;維持肥大細胞的穩定性 |
| 心理健康 | 介入措施:心理治療 | 主要可以增強自然殺手細胞(NK細胞)的活性,並維持NK細胞的免疫監視能力。 | 促進T細胞的增生和活化;促進抗體產生 | 維持或增強NK細胞的細胞毒殺活性;恢復樹突狀細胞的功能;抑制肥大細胞的功能和浸潤。 |
| 充足的睡眠 | 介入措施:維持充足的睡眠 | 增強適應性免疫功能,促進免疫記憶的形成,並維持先天性免疫系統的功能。 | 促進抗原特異性CD4+ T細胞數量的增加和免疫記憶的形成;促進抗體的產生 | 支持NK細胞的活性 |
#免疫編輯正常化
#免疫檢查點抑制劑
#自然殺手細胞
#免疫清除
#免疫平衡
#免疫逃逸
#免疫細胞治療
#免疫治療
#陳駿逸醫師
#台中市全方位癌症關懷協會
陳駿逸醫師醫療門診服務時段
https://mycancerfree.com/conta電腦斷層/
更多陳駿逸醫師的癌症衛教影片請連接https://www.youtube.com/@mycancerfree
更多腫瘤治療相關資訊 請連接”陳駿逸醫師 與你癌歸於好” https://mycancerfree.com


