血液腫瘤科/細胞治療中心/台灣細胞免疫醫學會 陳駿逸醫師
三陰性乳癌因缺乏雌激素受體、黃體素受體及人表皮生長因子受體2(HER2)的表達,化療長期以來是其核心治療手段。三陰性乳癌因為惡性度高、易轉移復發,早期三陰性乳癌患者的標準化治療中,術前輔助化療化療為首選方案,但約50%的患者於後續的手術當下仍存在有殘留腫瘤病灶。此類患者預後不佳,且大約有35%的三陰性乳癌患者會在術後兩年內出現疾病復發。目前針對三陰性乳癌患者,術前輔助化療化療結合免疫治療是現今國際標準趨勢。
透過術前將小紅莓、紫杉醇合併免疫藥物pembrolizumab(吉舒達)治療,將免疫藥物 Pembrolizumab加入術前前導性化療已成為目前的國際標準治療準則。這項療法的主要目標是提高「病理完全緩解率 (pCR)」可大幅縮小腫瘤、提升保留乳房機會,並可以提高達到病理學上腫瘤完全緩解(pCR)狀態,可以將pCR提高,即手術後切除組織中找不到癌細胞) 從約 51.2% 提升至 64.8%。顯著降低近約 37% 的疾病惡化或復發風險。進而降低復發風險並延長存活期,接受此合併療法的患者五年整體存活率大約為 86.6%,優於單純只化療組。。若在手術前接受輔助化療後病理檢查仍有殘存腫瘤 (Residual Disease),亦即是術前輔助化療後未達到病理學上腫瘤完全緩解(堅稱non-pCR),而口服化療藥物Capecitabine (截瘤達) 已被多項臨床試驗證實為標準的術後受輔助化療方案。
目前臨床中依賴的殘餘腫瘤負荷(簡稱RCB)評分,僅能靜態評估術前接受輔助化療後手術切除時的局部病灶範圍,無法精準地區分哪些患者體內仍存在有微小殘留病灶(簡稱MRD)並且於最終會導致三陰性乳癌的復發。
發表於2026年Clinical Cancer Research期刊之TRICIA試驗的研究成果。該研究探討術前輔助化療後未達到病理學上腫瘤完全緩解(堅稱non-pCR)的高復發風險之三陰性乳癌,借助ctDNA檢測,對三陰性乳癌患者手術前後輔助化療及capeciatbine輔助治療全療程進行了連續ctDNA動態追蹤。TRICIA試驗系統性驗證了ctDNA在三陰性乳癌中復發風險分層與療效監測中的臨床應用價值,為三陰性乳癌輔助治療的精准升降階梯決策提供了明確的科學實證。
ctDNA 檢測(Circulating Tumor DNA,循環腫瘤 DNA)是一種被稱為「液態切片」的新型癌症輔助檢測工具。它透過抽血來捕捉體內癌細胞凋亡或壞死後釋放到血液中的 DNA 片段。這項檢測與癌症傳統影像檢查最大的不同在於,它能比影像更早發現分子層級的變化:
指導癌症用藥: 透過 (NGS 次世代基因定序)同時分析多個癌症基因,協助醫師挑選合適的標靶藥物或免疫療法。
術後追蹤與 MRD 監測: 評估手術後體內是否仍殘留極微量的癌細胞(即MRD/微小殘留病灶),提早預警復發風險。
監測抗藥性: 定期抽血監測 ctDNA 變化,能即時發現腫瘤是否產生基因突變而導致現有治療失效。
如上所述,儘管ctDNA檢測被認為是檢測MRD的有效工具,但其在三陰性乳癌輔助療的領域仍存在顯著的科學空白。目前針對non-pCR這一超高復發風險之人群,術前接受輔助化療結束後、於後續手術前這一關鍵時間點上的ctDNA檢測之預後價值缺乏有公信力的驗證;且術前接受輔助化療後,針對non-pCR這一超高復發風險之人群,在術後輔助Capecitabine治療的全程,ctDNA檢測之ctDNA的變化及其與藥物療效的關聯之間,也缺乏關鍵性研究資料;而三陰性乳癌本身存在極高的基因突變異質性(除TP53為常見的基因共有突變外,極少有共同性突變),當前固定基因檢測極易出現漏掉的,臨床亟需兼具高靈敏度與高適配性的ctDNA的檢測方案。
TRICIA是一項在加拿大三家醫療中心所開展的多中心真實世界研究,共收錄92例,術前接受輔助化療結束後證實為non-pCR、高復發風險之三陰性乳癌患者。系統性評估ctDNA檢測的臨床價值,研究設定了四個核心ctDNA檢測的時間點:T1(術前接受輔助化療結束後/手術前)、T2(術後早期/術後輔助Capecitabine治療啟動前)、T3(術後輔助Capecitabine的治療期間)及T4(術後晚期/術後輔助Capecitabine治療結束後)。
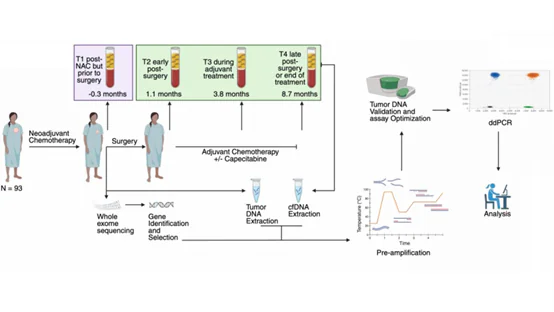
TRICIA研究流程圖
通過對262份血漿樣本的系統性追蹤與分析,研究全面證實了ctDNA檢測的在non-pCR 高復發風險之三陰性乳癌患者中的臨床價值:
- T1(術前接受輔助化療結束後/手術前):ctDNA檢測具備極佳強的預後分層能力
在64份T1時間點檢測樣本中,ctDNA結果為陽性患者的復發率達64%,而ctDNA陰性患者僅為5%(P<0.001)。該時間點對復發預測的敏感性為97%、特異性為54%、陰性預測值高達95%。生存資料分析顯示,T1 ctDNA陰性患者的5年無復發生存率和整體存活率均達95%(死亡風險降低94%,);而ctDNA陽性患者的5年整體存活率只有35%。
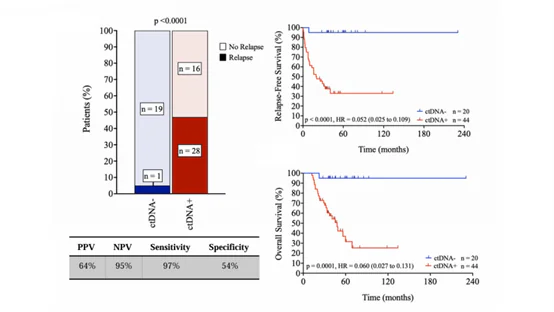
- ctDNA檢測可以在RCB的評分基礎上進一步精準地進行中高風險之分層
在預後最差的RCB 3級(有廣泛殘留病變)患者中,ctDNA檢測效能達100%: 所有T1 時間點之ctDNA結果為陽性患者均會出現三陰性乳癌的復發,所有ctDNA陰性患者均呈現無三陰性乳癌疾病的存活。在合併分析RCB 2級和RCB 3級患者時,T1 時間點的ctDNA結果為陰性患者的5年整體存活率為90%,而ctDNA結果為陽性患者的整體存活率只10%,證實ctDNA結果確實可以有效區分出有廣泛殘留病灶但卻無生物學侵犯性的患者亞群。(如下圖)
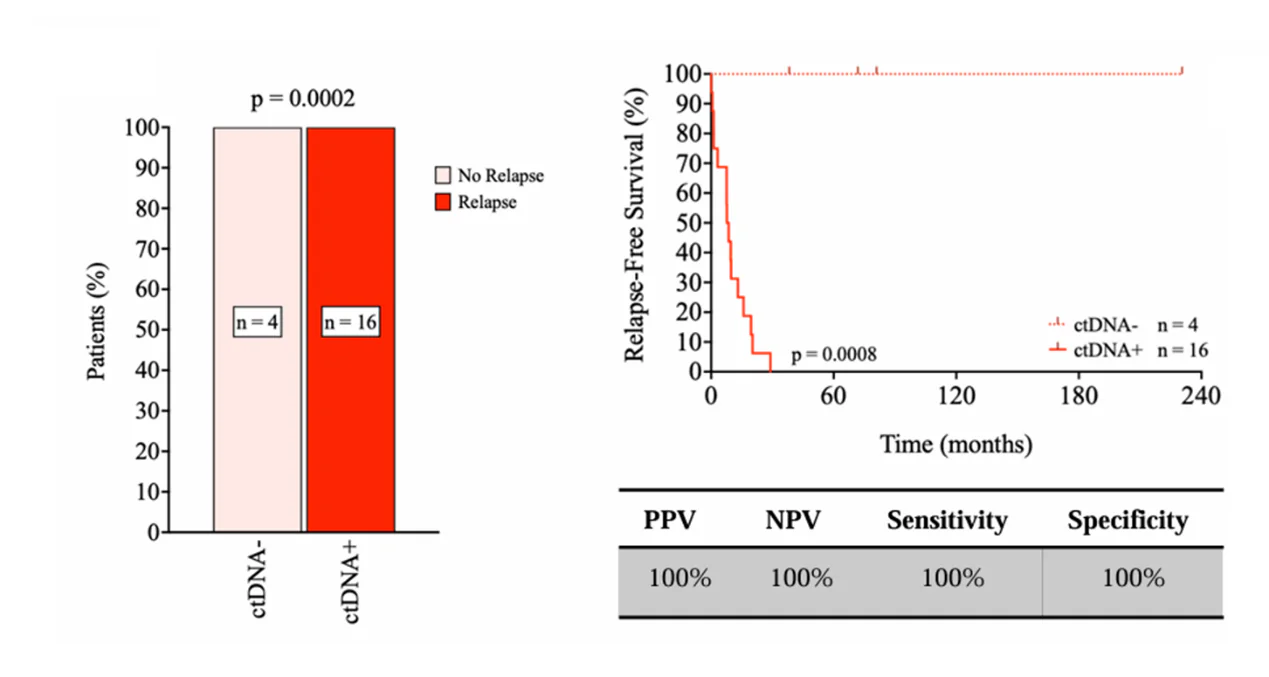
RCB 3級患者根據ctDNA結果所分層的復發情況與無癌症復發之存活時間的結果
- 手術可以顯著降低ctDNA的水平,術後早期的ctDNA檢測容易受到手術創傷所干擾
在T1/T2配對的樣本分析中,術後ctDNA之豐度會較術前而言,整體下降了91%,下降幅度與RCB分級呈現負相關。但同時發現,手術的創傷會導致正常組織釋放大量游離DNA(即cfDNA),稀釋原本低豐度的ctDNA信號,致使術後早期(T2時間)之ctDNA檢測的靈敏度和預測效能均弱於T1時間點(術前接受輔助化療結束後/手術前)。
- 術後ctDNA的檢測可提前12個月預測癌症的復發,T4(術後晚期/術後輔助Capecitabine治療結束後)的ctDNA檢測的檢測臨床價值最高
術後任意時間點ctDNA檢測結果陽性對癌症復發預測的敏感性達92%,且較臨床復發的中位時間可以提前12個月被發現,為臨床早期處置提供了關鍵視窗期。在術後各時間點中,且T4時間扁(術後晚期/術後輔助Capecitabine治療結束後)的預後評估價值是最強的:ctDNA檢測的結果為陽性患者其復發率為36%,ctDNA檢測的結果為陰性患者僅11%;且於T4時間點之 ctDNA檢測的結果為陰性患者的5年整體存活率可以高達100%。在整個追蹤期中,97%的復發患者在臨床確診有癌症復發前, ctDNA檢測的結果均可為陽性。
- ctDNA檢測得狀態是non-pCR之三陰性乳患者最強的獨立預後因素
多因素Cox回歸分析顯示,在校正RCB評分、是否接受術後輔助Capecitabine治療等變數後,T1(術前接受輔助化療結束後/手術前)時間點之ctDNA檢測的結果為陽性是患者復發的最強獨立預後因素(HR=24.7)。
- 術後輔助Capecitabine治療可以造成ctDNA清除,清除狀態與良好預後高度相關
在T2(術後早期/術後輔助Capecitabine治療啟動前)時間點之ctDNA檢測的結果為陽性的患者中,接受術後輔助Capecitabine治療的患者有41%在T4(術後晚期/術後輔助Capecitabine治療結束後)時間點實現ctDNA完全清除,而未接受該藥物治療的患者清除率只有9%(P<0.0001)。從預後角度看,接受術後輔助Capecitabine治療若達到ctDNA清除的患者,期癌症復發率僅15%,5年整體存活率可以高達100%(如下圖6;而ctDNA狀態持續還是陽性的患者復發率為37%,5年整體存活率只有52%。在接受術後輔助Capecitabine治療未達到ctDNA清除的患者中,最終復發者的ctDNA豐度在治療期間則會呈持續顯著升高的趨勢。
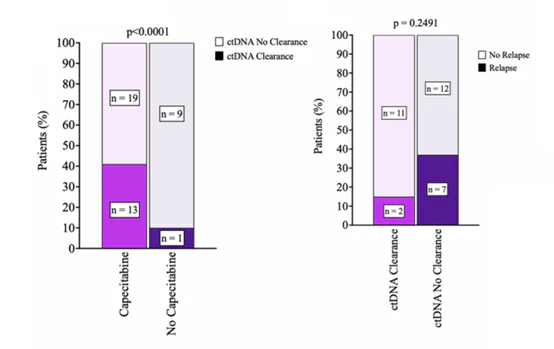
左圖:接受/未接受術後輔助Capecitabine治療患者的ctDNA清除比例;右右圖:T2-T4期間ctDNA狀態持續陽性或清除患者的癌症復發/三陰性乳患者無復發情況
TRICIA研究的結果提供了ctDNA的全療程之檢測可以協助優化三陰性乳患者臨床治療抉擇提供了直接的參考,解決了長期以來non-pCR三陰性乳患者患者輔助治療是否過度或不足的臨床問題。
在臨床治療的決策層面,該研究為輔助治療的降階梯策略提供了時證醫學證據。鑒於T1(術前接受輔助化療結束後/手術前)時間點之ctDNA檢測的結果為陰性的non-pCR三陰性乳患者,期癌症復發風險極低(陰性預測值達95%),該部分患者未來可能有機會免除術後輔助Capecitabine的治療,從而避免85%接受術後輔助Capecitabine治療無法獲益的患者需要承受嚴重的藥物副作用。同時,對於T1(術前接受輔助化療結束後/手術前)時間點之ctDNA檢測的結果為陽性、尤其是RCB評分為2/3級的三陰性乳患者,其極高的復發風險提示了可能需要進一步採取治療升階梯策略。此外,ctDNA的動態清除軌跡可作為術後輔助Capecitabine治療療效的早期替代終點,幫助臨床醫生可以儘早評估治療有效性,為治療無效的患者需要及時更換其他治療方案提供了決策證據。
未來仍需開展根據ctDNA之檢測結果指導的三陰性乳患者之治療決策的前瞻性干預性隨機對照試驗,以最終確立ctDNA之檢測臨床應用的基準。此外,未來還可以探索將ctDNA動態的變化與RCB評分、影像學特徵及分子亞型進行深度整合,構建多維度的ctDNA之檢測聯合預後之模型。
小結
TRICIA試驗首次系統性驗證了基於靶向預擴增的個體化ddPCR ctDNA檢測技術,在non-pCR三陰性乳腺癌患者全程治療中的預後評估與療效預測價值。該研究明確了新輔助化療後至術前(T1)是預後評估的最佳窗口期,並證實輔助治療期間ctDNA的動態清除狀態可準確反映卡培他濱在體內的抗腫瘤活性。該研究為三陰性乳腺癌從標準化輔助治療模式,向基於ctDNA指導的個體化精准治療模式轉變提供了高品質的臨床證據。
#ctDNA
#Circulating Tumor DNA
#循環腫瘤 DNA
#癌症
#三陰性乳癌
#TNBC
#免疫藥物
#Pembrolizumab
#吉舒達
#術前輔助化療
#陳駿逸醫師
#免疫治療
#台中市全方位癌症關懷協會
陳駿逸醫師醫療門診服務時段
https://mycancerfree.com/contact/
更多陳駿逸醫師的癌症衛教影片請連接https://www.youtube.com/@mycancerfree
更多腫瘤治療相關資訊 請連接”陳駿逸醫師 與你癌歸於好” https://mycancerfree.com

