血液腫瘤科/細胞治療中心/台灣細胞免疫醫學會 陳駿逸醫師
骨肉瘤的藥物治療史
自從Alex Bowyer 在 1805 年發現骨肉瘤以來,過去兩個世紀來治療方法已有顯著進步。歷史上,直到 19 世紀中葉和 20 世紀初,將受影響的肢體進行截肢是標準治療方法。然而,由於醫療技術有限和衛生條件差,接受截肢的患者往往可能會面臨高風險的敗血症和其他手術部位感染。
隨著 20 世紀初手術技術的改進,手術後感染率降低;然而,由於轉移風險持續存在,死亡率仍然很高。在 20 世紀初至中葉,放射治療變得流行,儘管最初由於準確定位癌細胞有其限制,它在對骨肉瘤的治療中顯示出有限的效果。
到了 1970 年代,標準的治療變得多元化。多藥物化療的引入顯著強化了腫瘤縮小,並迅速成為最廣泛採用的治療策略。化療允許足夠的腫瘤縮小,從而促進了「保留肢體手術」的發展,這很快成為完全截肢的常見替代方案。這種方法允許許多患者保留肢體,僅僅移除少量的骨組織。在 21 世紀,最常見的治療方案包括新藥物治療後,接續腫瘤的手術切除。常見的化學治療藥物包括cisplatin、doxorubicin和methotrexate,這些藥物都主要是針對對腫瘤細胞生存和增殖至關重要的關鍵分子途徑。
骨肉瘤新的治療方法
基因治療:
隨著醫學科學的持續進步,骨肉瘤的新治療方法展現出顯著的潛力。這些新型治療方法的先鋒是基因治療,它透過針對促進癌症生長和轉移的特定遺傳和分子因素來作。常見的靶點包括抑癌基因、參與藥物敏感性途徑的途徑,以及能夠促進損壞 DNA 片段修復的基因編輯系統,例如 CRISPR/Cas9。
針對腫瘤抑制基因的基因治療,是能夠將功能性基因副本引入宿主基因組,幫助恢復正常細胞週期調節和生理性凋亡。在骨肉瘤中,常見的改變型腫瘤抑制基因是 TP53,其突變會干擾 G1 細胞週期的檢查點。這不僅促進腫瘤生長,也增加了癌細胞對於維持 DNA 完整性的 G2 檢查點的依賴性。
針對改變藥物敏感性途徑的基因治療也顯示出前景,因為許多骨肉瘤細胞能夠獲得突變或表達能夠增強藥物抗性的蛋白質。這種抗藥性的一個主要來源是特定的外泌體(一種通常參與細胞間溝通和環境調節的小型細胞外囊泡)。在癌細胞中,特定的外泌體可以分泌化療,上調藥物外排泵(如 P-糖蛋白,P-gp)劑如多柔比星,並將多藥抗藥性的mRNA 從抗藥癌細胞轉帶到敏感的癌細胞,導致抗藥性的傳播。有趣的是,使外泌體成為有效抗藥性載體的相同機制,也使其成為基因治療的很有前景的目標。外泌體具備優良的特性,如小尺寸、良好溶解度、低毒性以及長的半衰期。程式化外泌體已被探索作為 miRNA 的傳送系統,研究顯示它們通常比現有方法更具選擇性和更少的細胞毒性(可能是由於外泌體膜蛋白與腫瘤細胞膜的相互作用)。2022 年的研究證明,載有 miR-665、miR-22-3p的外泌體反而能夠在體內和體外抑制骨肉瘤的發展,同時保持良好的安全性和效率特徵。儘管外泌體有其優點,但仍面臨到一些限制,主要是難以在足夠的數量和純度中分離出它們,以及缺乏數據識別哪些特定外泌體在癌症類型中最有效。此外,目前仍不清楚其他納米粒子傳的送系統,例如高細胞通透性膠束,是否最終能證明更有效。雖然外泌體共享許多有益的特徵,但它們缺乏實驗室工程納米粒子的專一性。
基因治療也讓研究人員能夠利用 CRISPR/Cas9 技術進行精準的基因組編輯,並識別出藥物抗藥性基因。這使得可以針對性地修改導致骨肉瘤的發展和藥物抗藥性的基因,進而改進治療成績。CRISPR 以多種方式對抗癌症,其中經典方法是設計單導向 RNA(sgRNA)來結合特定的 DNA 序列,如下圖所示。這段 RNA 引導 Cas9 蛋白到達目標位點,在那裡它會切割 DNA的雙鏈。然後細胞啟動修復的機制。CRISPR 可用於去活化致癌基因、中斷免疫檢查點基因,或直接在癌症細胞中引發DNA的雙鏈斷裂。2023 年的研究顯示,CRISPR 靶向 PLK1(為G2/M 檢查點的終極調節因子),當成功敲除了該基因,並在體外和體內抑制了骨肉瘤細胞的增殖。
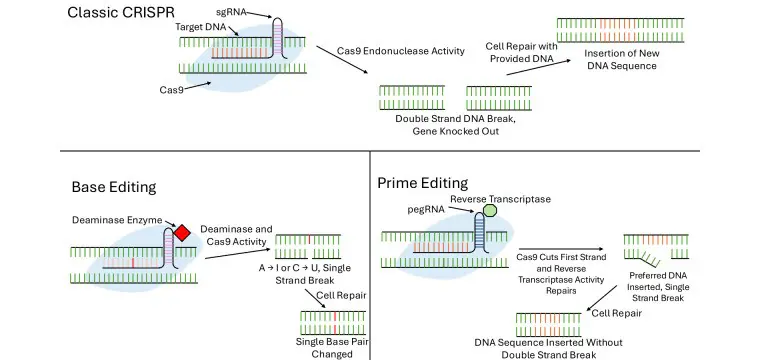
CRISPR/Cas9、基序編輯及主要編輯機制之示意圖,比較三種技術在組成、進程及結果上的差異
更先進的基因編輯策略,包括:基序編輯(base editing)和主編輯(prime editing)。基序編輯能夠使用 Cas9 去氨基酶融合蛋白,將一種核苷酸基轉換為另一種,這可以將胞嘧啶轉換為尿嘧啶、或是腺嘌呤轉換為次黃嘌呤。此過程使用編輯過的鏈作為模板來誘導修復。雖然基序編輯引入的錯誤較少,例如轉位或重排,且適合單一核苷酸的修改,但它無法插入 DNA 片段或進行基因敲除,限制了其使用範圍。
而Prime editing 解決了這些限制。利用一種 prime editing 指導 RNA (pegRNA)、一種反轉錄酶、一種 Cas9 融合蛋白和一種 nicking 去指導 RNA 來插入 indels 或點突變。在結合到目標位點、並切斷一條 DNA 鏈後,反轉錄酶合成了新的序列,當互補鏈被切斷後,這個新序列就會被複製過去。這種技術比起基编辑更具多樣性,也比傳統的 CRISPR 具有更高的保真度,因為它避免了雙鏈的斷裂。儘管設計 pegRNAs仍然是一個挑戰,但 prime editing 已經在多個模式生物中顯示出成功,並對個人化醫學充滿希望。
除了直接編輯外,CRISPR的篩選也用於識別與藥物抗藥性相關的表型與基因。這涉及到敲除特定的基因,並觀察藥物暴露後的細胞存活情況。存活的細胞通常帶有與抗藥性相關的基因突變,接著可以在細胞株中進行驗證,以判斷抗藥性是藥物特定的、還是可以全盤化的。雖然基因治療具有巨大的前景,但在獲得美國 FDA 批准之前,需要進一步的臨床試驗來評估長期安全性、傳送效率以及治療效能。
免疫療法:
免疫療法在治療骨肉瘤方面上已顯示出潛力,特別是在進展性或有抗藥性病例中,傳統療法經常無法達到治療效果。骨肉瘤以其逃避免疫系統的能力著稱,主要是通過表達免疫檢查點蛋白(如:PD-L1),這些蛋白抑制免疫活性並使癌細胞無限制地增殖。
在胃癌細胞中,PD-L1 已被證明在通過間質細胞的重塑、細胞信號的傳遞、可溶性因子分泌和免疫細胞分化來調節免疫抑制和腫瘤的侵襲作用。PD-L1也可能在骨肉瘤中扮演類似的角色。免疫療法通過利用宿主免疫系統來識別和摧毀腫瘤細胞來對抗這種免疫逃逸,特別是重新激活 T 細胞,像免疫檢查點(PD-L1 和 CTLA-4) 抑制劑,如pembrolizumab 和 nivolumab 這樣的藥物,可以中斷免疫抑制信號的級聯,從而重激活 T 細胞以發動抗腫瘤反應。
另一個有潛力的 T 細胞再活化的靶點是 TIM-3免疫檢查點,這是一種表達於多種免疫細胞表面的蛋白質。在骨肉瘤腫瘤微環境中,TIM-3 與 Gal-9 結合可以誘導 CD4 + 和 CD8 + T 細胞的凋亡。阻斷 TIM-3 已被證明可增以加骨肉瘤模型中腫瘤浸潤 CD8 + T 細胞的數量和活性。一項 2021 年的 I/II 期試驗評估了 sabatolimab(一種抗 TIM-3 免疫檢查點抑制劑)單獨及與 spartalizumab(一種抗 PD-1 免疫檢查點抑制劑)聯合使用於晚期固體腫瘤患者。雖然 sabatolimab 單獨顯示出有限的療效,但聯合治療顯示出有希望的活性且不良反應最小。儘管需要進一步的研究,TIM-3 代表了一個有希望的靶點,可用於未來的聯合治療。
嵌合抗原受體 (CAR) T 療法在血液學惡性腫瘤中已顯示出療效,但在實體癌症中的療效有限,這是因為其腫瘤微環境中的障礙,例如:密實的間質組織、缺氧狀態和免疫抑制細胞群。CAR T 細胞療法涉及從患者或相容的捐贈者收集 T 細胞,並進行基因改造以針對特定的腫瘤相關抗原。基本的 CAR 結構包括抗原結合域、鉸鏈、跨膜域和細胞內信號傳遞域。進步包括添加共刺激域以改善活化、可誘導轉基因以提高安全性,以及專用受體以精確針對和信號傳遞。
儘管有這些創新,CAR T 細胞單獨治療對於骨肉瘤等實體癌症仍然效果不佳。一項 2024 年的第一期試驗研究了針對 GD2 的 CAR T 治療(此前已被證明對神經母細胞瘤安全),但發現骨肉瘤患者沒有出現客觀的治療反應。然而,部分患者經過 90 天後病情穩定,並出現可測量的 CAR T 細胞擴增。儘管這些發現令人鼓舞,但在 CAR T 治療成為骨肉瘤可靠選項之前,仍需進一步的優化。
另一條正在研發的免疫治療途徑是針對 CD47-SIRPα(don’t eat me)免疫檢查點,它具有調節免疫吞噬的作用。腫瘤細胞可以過表達 CD47 來模擬「自我」信號,從而避免被巨噬細胞的破壞。針對 SIRPα的單株抗體 BMS-986351 已顯示出治療潛力,可以加強巨噬細胞所介導的吞噬作用,尤其是在與包被抗體結合時。然而,由於 SIRPα在身體各處的會廣泛表達,提高選擇性仍然是一個關鍵挑戰。一項 2025 年進行的早期試驗評估了 margolimab(一種 CD47 免疫檢查點抑制劑)和 cetuximab(一種 EGFR 阻斷劑)在 KRAS 野生型大腸直腸癌中的結合使用。雖然不具體針對 OS,但結合使用顯示出耐受性和抗腫瘤活性,表明 CD47 阻斷可能具有更廣泛的應用性。
其他免疫療法策略,如:癌症疫苗,也正積極研究中。這些方法中特別是涉及樹突細胞活化的方法,於基礎及臨床試驗中已顯示出不一致性的結果,突顯了持續改進的必要性。免疫療法的主要挑戰仍然是有關治療的毒性。免疫系統過度活化可能導致嚴重的副作用,包括消化系統、內分泌系統和皮膚毒性。更嚴重的免疫相關不良事件,包括了神經毒性、心臟毒性和肺毒性。如果出現顯著毒性,治療通常會中斷,並可能施用類固醇或免疫抑制劑。這些不良反應被認為源於免疫系統攻擊與腫瘤細胞有共同分子標記的正常組織,導致類似自身免疫的反應。
腫瘤微環境在免疫療法的抗藥性和有效性中扮演著關鍵的角色。在骨肉瘤中,腫瘤微環境,包含了癌細胞、間質成分、血管、可溶性因子以及免疫細胞(如成骨細胞、破骨細胞、巨噬細胞和 T 細胞。由於 TGF-β和 IL-10 等分子會抑制免疫反應進而促進腫瘤的生長,會讓腫瘤微環境具有高度免疫抑制性。此外,腫瘤微環境中的細胞,包括腫瘤相關巨噬細胞(TAM)、NK 細胞和調節性 T 細胞,是可以被重新編程以支持免疫的逃逸。由於這些細胞表達 PD-1 和 CD47 等檢查點蛋白。其他癌症的轉錄組學和功能分析可以應用於骨肉瘤的腫瘤相關巨噬細胞或其他免疫細胞類型,為靶向免疫療法開發提供新的途徑。
標靶治療:
另一個在治療骨肉瘤上被廣泛測試的科學領域是標靶治療-酪氨酸激酶抑制剂(TKIs)。對於癌症細胞已進入晚期、已出現轉移或對其他治療特別具抗藥性的 骨肉瘤病例,標靶治療可能是有用的,治療的原則是透過針對與腫瘤生長和轉移有關的特定細胞通路來運作。標靶治療會與酪氨酸激酶的 ATP 結合位點上的 ATP 競爭,降低酪氨酸激酶磷酸化並抑制其活性。大多數標靶治療的作用目標是多個通路,標靶治療最常目標的五種受體是:KIT、血管內皮生長因子受體(VEGFRs)、RET、血小板衍生生長因子受體(PDGFRs)和纖維母細胞生長因子受體 1(FGFR1)。另一項研究也顯示,標靶治療anlotinib可以增加骨肉瘤細胞對化療的敏感性,方法是增加細胞在 G2/M 期的比例。
KIT 是一種以幹細胞因子為配體的 RTK。當與其配體結合時,KIT 會觸發許多對分化、增殖和移動等重要細胞過程至關重要的信號傳遞路徑。一些研究顯示 KIT 表達在骨肉瘤中明顯。另一項研究發現,KIT陽性的骨肉瘤對化療的反應不如預期。然而,儘僅僅靶向 KIT 並非骨肉瘤的有效治療方法。
標靶治療藥物的一個常見目標是 VEGF。在骨肉瘤的患者中,VEGF 和 VEGFA 的表達與更差的無病生存率和總生存率有關。在 IHC 研究中,VEGF 表達在 63–74%的骨肉瘤樣本中被檢測到。在另一項下一代测序(NGS)研究中,41.2%的轉移性/復發的骨肉瘤樣本被顯示出表達 VEGF。抑制這個基因可以防止血管生成,即新血管的形成,並且是腫瘤形成六大標誌之一。抑制血管生成將阻止腫瘤增長並改善患者結果,因此,VEGF 是的骨肉瘤治療中的關鍵目標。
另一種常在骨肉瘤患者中過表達的 RTK 是 FGFR。FGFRs 調節神經系統控制、器官發生和組織修復等]。FGFR1 在 74%的骨肉瘤樣本中表達,使其成為 TKIs 的可能又一藥物作用的靶點。
標靶治療藥物的另一個常見目標也包含間葉細胞-上皮細胞轉換 (MET) 因子與 PDGFR,它們參與對腫瘤生長與增殖至關重要的途徑。在診斷為骨肉瘤的患者中,MET 的過度產生往往導致較差的病人結果,並增加轉移的機率。而PDGFR 在多種生物過程中發揮作用,包括細胞生長、存活、移動與分化。它是能與 PDGFs(分泌蛋白質,參與腫瘤微環境與間質細胞中的信號傳遞)結合的受體家族的一部分。許多正在進行臨床測試的標靶治療藥物的一個常見目標旨在同時標靶 MET 與 PDGFR。像cabozantinib、 regorafenib與 pazopanib等藥物同時標靶 MET 與 PDGFR 途徑,使其對於具有雙重途徑失調的骨肉瘤病例具有重要價值。
RET 是另一種在卵巢癌、肺癌中起作用的。RET 被認為會促進腫瘤的轉移行為,同時與化療抗藥性的增加有關。因此,RET 成為許多標靶治療藥物的靶點。但 IGF-R(類胰島素生長因子受體)被認為可促進癌細胞生長、抑制細胞凋亡,從而促使腫瘤生長,其主要作用途徑為 PI3K 和 MAPK 通路。
AXL 在骨肉瘤中被發現表達率很高,且與不良預後呈正相關。在一項用於老鼠模型的研究中發現,AXL 抑制能顯著減少 MG63.2 肺轉移瘤的數量。在一項使用多靶點激酶抑制劑的臨床試驗中,當抑制 AXL 時,部分患者出現了陽性反應]。儘管這是一個很有前景的結果,但尚未有單靶點研究探討抑制 AXL 對患者結果的影響。在大多數骨肉瘤組織中,AXL 表達率很高。其敲低與抑制骨肉瘤細胞增殖及誘導其凋亡相關。一項前期臨床試驗也發現,在一種高度轉移性的骨肉瘤細胞系中 AXL 表達過度,而其抑制能減少細胞增殖、侵襲和轉移。
這些標靶治療藥物在小型試驗中的成功顯示了對骨肉瘤治療的有效性,然而,更廣泛的使用將取決於確認其與目前標準治療相比的有效性的第三期試驗結果。透過同時抑制腫瘤血管生成、腫瘤細胞增殖和轉移相關通路,這些藥物可以潛在地改善侵略性和轉移性骨肉瘤患者的結果。儘管這些藥物也可以抑制多個靶點,但它們可能對患者產生未知影響,例如:一些研究報告指出,骨肉瘤會影響身體的多個器官,或可能產生心血管副作用,如高血壓、心房纖維性心律不整、減少心臟功能、心力衰竭甚至猝死
#骨肉瘤
#中央型骨肉瘤
#髓腔內骨肉瘤
#表面型骨肉瘤
#周邊型骨肉瘤
#化學治療藥物
#cisplatin
#doxorubicin
#methotrexate
#基因編輯
#CRISPR/Cas9
#miR-665
#miR-22-3p
#外泌體
#胞外體
#免疫治療
#免疫檢查點抑制劑
#CD47-SIRPα
#margolimab
#CAR T
#細胞療法
#標靶治療
#陳駿逸醫師
#台中市全方位癌症關懷協會
陳駿逸醫師醫療門診服務時段
https://mycancerfree.com/contact/
更多陳駿逸醫師的癌症衛教影片請連接https://www.youtube.com/@mycancerfree
更多腫瘤治療相關資訊 請連接”陳駿逸醫師 與你癌歸於好” https://mycancerfree.com